
题目列表(包括答案和解析)
①溶解 ②加BaCl2溶液 ③过滤 ④洗涤沉淀 ⑤烘干 ⑥称量等,最后计算结果。
问:
(1)将BaCl2溶液加入样品溶液中时,怎样判断沉淀是否完全?
(2)过滤后,为何要用蒸馏水洗涤沉淀?若不洗,对实验结果有何影响?
(3)如何判断沉淀已经洗净?
(4)若取样品为1.612g,最后称得沉淀为2.33g,计算K2SO4和Na2SO4的质量分数。
为了测定K2SO4和NaSO4混合物中各组分的质量分数,分析人员称取该混合物样品Ag并经过如下操作:
①溶解 ②加BaCl2溶液 ③过滤 ④洗涤沉淀 ⑤烘干 ⑥称量等,最后计算结果。
问:
(1)将BaCl2溶液加入样品溶液中时,怎样判断沉淀是否完全?
(2)过滤后,为何要用蒸馏水洗涤沉淀?若不洗,对实验结果有何影响?
(3)如何判断沉淀已经洗净?
(4)若取样品为1.612g,最后称得沉淀为2.33g,计算K2SO4和Na2SO4的质量分数。
①溶解②加BaCl2溶液 ③过滤 ④洗涤沉淀 ⑤烘干⑥称量等,最后计算结果。问:
(1)将BaCl2溶液加入样品溶解液中时,怎样判断沉淀是否沉淀完全?
(2)过滤后,为何要用蒸馏水洗涤沉淀?若不洗涤,对实验结果有何影响?
(3)如何判断沉淀是否已洗涤干净?
(4)若称取样品为1.612g,最后称得沉淀为2.33g,计算K2SO4和Na2SO4的质量分数。
碱式碳酸铜是一种用途广泛的化工原料。工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl-)制备,其制备过程如下:

Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
|
物质 |
Cu(OH)2 |
Fe (OH)2 |
Fe (OH)3 |
|
开始沉淀pH |
4.2 |
5.8 |
1.2 |
|
完全沉淀pH |
6.7 |
8.3 |
3.2 |
(1)氯酸钠的作用是 ;滤渣的主要成分是 (写化学式)。
(2)调节反应A后溶液的pH范围应为 。可以选择的试剂是 (填序号)。
a.氨水 b.稀硫酸 c.氢氧化钠 d.碳酸铜
(3)反应B的温度如过高,则所得蓝绿色产品中可能会出现的杂质是 。(写化学式)
(4)过滤得到的产品洗涤时,如何判断产品已经洗净? 。
(5)将Na2CO3溶液滴入到一定量CuCl2溶液中得到沉淀。
① 若沉淀只有CuCO3,则相应的离子方程式为 。
② 若沉淀只有Cu(OH)2,用相应的离子方程式表示其过程 。
③ 若生成Cu(OH)2和CuCO3的混合物(即碱式盐)。则说明 。
(6)碱式碳酸铜组成可表示为:aCuCO3•bCu(OH)2•cH2O,现通过下列方案测定其组成。步骤如下:
① 称量样品;② 高温分解;③ 测出CO2的质量;④ 测出水蒸汽的质量;⑤ 称量CuO。
请对上述测定方案作出评价。 。
碱式碳酸铜是一种用途广泛的化工原料。工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl-)制备,其制备过程如下: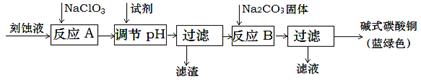
Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com