(2009?静安区一模)某学习小组利用下图所示装置进行“铁与水气反应”和其他实验(略去了夹持仪器).
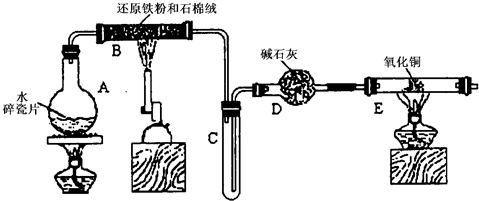
(1)仪器B的名称是
石英管或硬质玻璃管
石英管或硬质玻璃管
,石棉绒的作用是
增大铁与水蒸气接触面积,防止加热时固体喷入导管
增大铁与水蒸气接触面积,防止加热时固体喷入导管
.
(2)B中发生反应的化学方程式是
.
(3)加热E以前要对装置中的气体验纯,方法是:收集一试管气体,然后
将试管口靠近酒精灯火焰,弱发出噗的声音,说明气体纯净;若发生尖锐爆鸣声,说明气体不纯
将试管口靠近酒精灯火焰,弱发出噗的声音,说明气体纯净;若发生尖锐爆鸣声,说明气体不纯
.
(4)已知有反应:Cu
20+2H
+→Cu+Cu
2++H
20,则可用来检验反应后E中的红色固体中除Cu外是否含Cu
20,可用的试剂是
bc
bc
(填序号)
a.稀硝酸 b.稀硫酸 c.盐酸 d.浓硫酸
(5)在E后若再接二个盛碱石灰的干燥管(依次称为F和G),则还可用该装置测定水的组成或铜的相对原子质量.若反应前盛有药品的E、F的质量分别是bg、cg,反应后分别是dg、eg.
①水中元素的物质的量之比可表示为n(H):n(0)=
;若反应后E中除Cu外还含有另种还原产物Cu
20,则该比值将
无影响
无影响
(选填“偏大”“偏小”或“无影响”).
②若空的E管的质量为ag,加热后CuO完全还原为Cu,则铜的相对原子质量可表示为
.

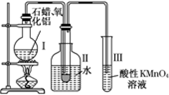 如何从石油中获得更多的轻质燃油一直是化学家探索的课题,将石油分馏得到的重油进行裂化可以获得更多的轻质燃油.
如何从石油中获得更多的轻质燃油一直是化学家探索的课题,将石油分馏得到的重油进行裂化可以获得更多的轻质燃油.
 实验室用固体NaOH配制0.5mol/L的NaOH溶液500mL,有以下仪器和用品有:
实验室用固体NaOH配制0.5mol/L的NaOH溶液500mL,有以下仪器和用品有: