
题目列表(包括答案和解析)
| |||||||||||||||||||||||||||||||||||||
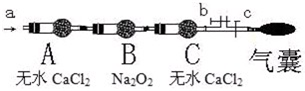
(1)由实验现象所得出的有关![]() 和
和![]() 反应的结论是:a.有氧气生成;b.________
反应的结论是:a.有氧气生成;b.________
____________________________________.
![]() 和
和![]() 反应的化学方程式是____________________.
反应的化学方程式是____________________.
(2)某研究性学习小组拟用下图中的装置进行实验,以证明上述结论.
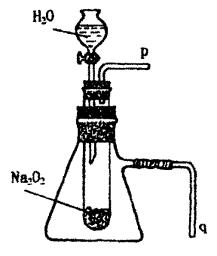
①用以验证结论a的实验方法是:
________________________________________________________________________.
②用以验证结论b的实验方法及现象是:
________________________________________________________________________.
(3)实验(2)往试管中加水至固体完全溶解且不再有气泡生成后,取出试管,往试管中滴入酚酞试液,发现溶液变红,振荡后,红色消褪.为探究此现象,该小组同学从查阅有关资料中得知:![]() 与
与![]() 反应可生成
反应可生成![]() ,
,![]() 具有强氧化性和漂白性.请设计一个简单的实验,证明
具有强氧化性和漂白性.请设计一个简单的实验,证明![]() 和足量
和足量![]() 充分反应后的溶液中有
充分反应后的溶液中有![]() 存在.(只要求列出实验所用的试剂及观察到的现象)
存在.(只要求列出实验所用的试剂及观察到的现象)
试剂:____________________________________________________.
现象:____________________________________________________.
某高一化学探究小组的同学设计实验探究0.5 mol/L NaOH溶液、0.5 mol/L 硫酸溶液、0.2 mol/L Na2CO3溶液两两相互反应的情况.
(1)配制0.50 mol/L NaOH溶液
①若实验中大约要使用100 mL NaOH溶液,至少需要称量NaOH固体________g;
②从下图中选择称量NaOH固体所需要的仪器(填字母):________,配制0.50 mol/L NaOH溶液还需要的仪器有________.
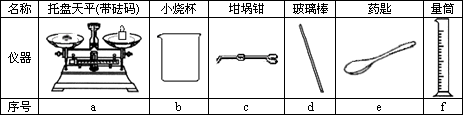
③在配制过程中,下列情况会导致溶液浓度偏高的是________.
A.容量瓶使用前经蒸馏水清洗后没有干燥
B.配制过程中未用蒸馏水洗涤烧杯和玻璃棒
C.俯视确定凹液面与刻度线相切
D.用敞口容器称量NaOH且时间过长
(2)探究相关反应
①将30 mL 0.2 mol/L Na2CO3溶液逐渐加入30 mL 0.5 mol/L H2SO4溶液中,看到的现象是________;
②将2~3滴酚酞溶液滴入60 mL NaOH溶液中,看到的现象是________,向该NaOH溶液中逐渐加入0.5 mol/L H2SO4溶液40 mL,最后所得溶液的溶质为________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com