
题目列表(包括答案和解析)
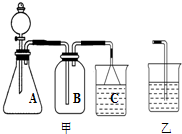 分析解答下列化学实验和计算问题:
分析解答下列化学实验和计算问题:| 233m1-142m2 |
| 233m1 |
| 233m1-142m2 |
| 233m1 |
露置的苛性钾经分析,其中含有的各种物质的质量分数分别为:H2O 7.62%,K2CO3 2.38%,KOH 90%。若将此样品1 g加入到1 mol·L-1的盐酸46.00 mL中,过量的盐酸用1.070 mol·L-1 KOH溶液恰好中和。蒸发中和后的溶液,可得固体()
A.3.43 g B.4.00 g
C.4.50 g D.无法计算
A.3.43 g B.4.00 g C.4.50 g D.无法计算
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com