
题目列表(包括答案和解析)
某教师用如下图所示装置做“稀硝酸的氧化性及NO的性质等”演示实验。图中1、2、3、4为止水夹。操作步骤如下:
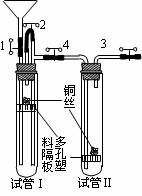
①检查装置的气密性;
②打开1、2、3、4,经漏斗加入稀硝酸,直至酸液充满试管I;
③关闭1、2,打开3、4,用酒精灯微热试管I,当铜丝表面有气泡产生时,立即撤去酒精灯;
④随着反应进行,I中液体会流入II并浸没隔板上的铜丝,此时立即加热试管II,即可看到II中有红棕色气体产生。当红棕色气体充满II后,立即关闭3;
⑤一段时间后,关闭4并撤去酒精灯,将试管II(连同塞子及止水夹3、4)浸入盛有冰水的大烧杯中。
试回答下列问题:
(1)步骤②中稀硝酸要充满试管I的目的是_______________________________ 。
(2)步骤③中发生反应的离子方程式为_________________________________________。
(3)步骤④中产生红棕色气体的化学方程式是_________________________________。
该步骤中关闭3产生的结果是___________________________________________。
(4)实验中观察到初始阶段步骤④中产生气体的速率明显快于步骤③,你认为其可能的原因是_____________________________________________。(写出一条即可)
(5)步骤⑤中可观察到的主要现象是_________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com