
题目列表(包括答案和解析)

请回答下列问题:
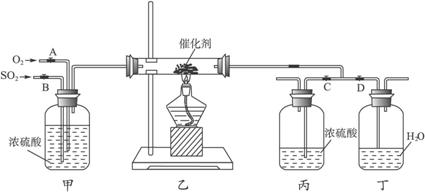
(1)写出FeS2与氧气反应的化学方程式:____________________________。
(2)从乙装置中出来的气体有__________________________________________。
(3)写出上图丙装置的作用__________________________________________。
(4)在装置乙的反应器内要求氧气的量要比二氧化硫的量多一倍左右,实验时你是如何控制与估计的?____________________________。
(5)接触法制硫酸过程中,若反应热都未被利用,则每生产1 ![]() 2SO3(g);ΔH=-98.3 kJ·mol-1的热量能在生产过程中得到充分利用(其他反应热不计),则每生产1
2SO3(g);ΔH=-98.3 kJ·mol-1的热量能在生产过程中得到充分利用(其他反应热不计),则每生产1
(6)本实验增加丁装置的目的是为了探究____________________________。
(7)本实验设计还存在的较明显缺陷是_______________________________。
请回答下列问题:
(1)写出FeS2与氧气反应的化学方程式:_______________。
(2)从乙装置中出来的气体有_______________。
(3)写出上图丙装置的作用______________________________。
(4)在装置乙的反应器内要求氧气的量要比二氧化硫的量多一倍左右,实验时你是如何控制与估计的?_______________。
(5)接触法制硫酸过程中,若反应热都未被利用,则每生产1 ![]() 2SO3(g);ΔH=-98.3 kJ·mol-1的热量能在生产过程中得到充分利用(其他反应热不计),则每生产1
2SO3(g);ΔH=-98.3 kJ·mol-1的热量能在生产过程中得到充分利用(其他反应热不计),则每生产1
(6)本实验增加丁装置的目的是为了探究______________________________。
(7)本实验设计还存在的较明显缺陷是______________________________。
Ⅰ下列说法不正确的是____ 。
A.可以利用某些炼钢废渣来生产磷肥
B.具有永久硬度的水主要用加热的方法来进行软化
C.硫酸工业中,在接触室安装热交换器是为了利用S03转化为H2S04时放出的热量
D.合成氨工业原料气净化时,常用碳酸钾溶液吸收除去二氧化碳
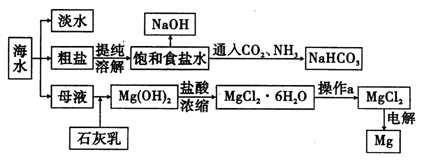
Ⅱ下图是某工厂对海水资源进行综合利用的示意图。

请回答下列问题:
(1)用离子交换膜电解饱和食盐水时,精制的饱和食盐水应该加入到 极室。
(2)已知在离子交换膜电解槽中,理论上每小时通过1安培的直流电,每槽可以产生1.492 g的烧碱,某工厂用300个电解槽串联生产8小时,制得32%的烧碱溶液(密度为1.342×103 kg/m3)113 m3,电解槽的电流强度1.45×l04 A,该电解槽的电解效率为 。
(3)示意图中制取NaHC03的化学方程式为 。
(4)有人提出直接加热Mg(OH)2得到Mg0,再电解熔融Mg0得金属Mg,这样可简化流程。请判断该方案是否可行,并说明理由 。
Ⅰ下列说法不正确的是____ 。
| A.可以利用某些炼钢废渣来生产磷肥 |
| B.具有永久硬度的水主要用加热的方法来进行软化 |
| C.硫酸工业中,在接触室安装热交换器是为了利用S03转化为H2S04时放出的热量 |
| D.合成氨工业原料气净化时,常用碳酸钾溶液吸收除去二氧化碳 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com