
题目列表(包括答案和解析)
|
到现在为止,已发现元素112种,把现在的元素周期表中所有的横行和纵行数相加其和为 | |
A. |
22 |
B. |
23 |
C. |
24 |
D. |
25 |
|
到现在为止,已发现元素112种,把现在的元素周期表中所有的横行和纵行数相加其和为 | |
A. |
22 |
B. |
23 |
C. |
24 |
D. |
25 |
| 序号 | 选用指示剂 | 选用滴定管 |
| A | 石蕊 | (乙) |
| B | 甲基橙 | (甲) |
| C | 酚酞 | (甲) |
| D | 酚酞 | (乙) |
实验编号 |
待测盐酸溶液体积(mL) |
滴定开始读数(mL) |
滴定结束读数(mL) |
| ① |
25.00 |
0.00 |
23.80 |
② |
25.00 |
1.00 |
24.78 |
| ③ |
25.00 |
0.22 |
24.04 |

 某学习小组的学生用标准浓度的氢氧化钠溶液测定未知浓度的盐酸溶液,
某学习小组的学生用标准浓度的氢氧化钠溶液测定未知浓度的盐酸溶液,| 序号 | 选用指示剂 | 选用滴定管 |
| A | 石蕊 | (乙) |
| B | 甲基橙 | (甲) |
| C | 酚酞 | (甲) |
| D | 酚酞 | (乙) |
实验编号 |
待测盐酸溶液体积(mL) |
滴定开始读数(mL) |
滴定结束读数(mL) |
| ① |
25.00 |
0.00 |
23.80 |
② |
25.00 |
1.00 |
24.78 |
| ③ |
25.00 |
0.22 |
24.04 |
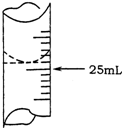 欲测定某NaOH溶液的物质的量浓度,可用0.1000mol?L-1HCl标准溶液进行中和滴定(用酚酞作指示剂).
欲测定某NaOH溶液的物质的量浓度,可用0.1000mol?L-1HCl标准溶液进行中和滴定(用酚酞作指示剂).| 实验序号 | 待测NaOH溶液的体积/mL | 0.1000mol?L-1HCl溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 0.00 | 26.11 |
| 2 | 25.00 | 1.56 | 31.30 |
| 3 | 25.00 | 0.22 | 26.31 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com