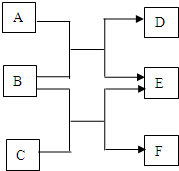
A、B、C、D、E、F六种物质均是由短周期元素组成的中学常见的化学物质.它们之间的转化关系如下图.
(1)若A、C、E均为氧化物,且E为有毒气体,B、D、F均为非金属单质,且D为气体,则:
①F的晶体类型为
原子晶体
原子晶体
; 1molC中含有
4
4
mol共价键;
②B与C反应生成E和F的化学方程式为
(2)若A、C、E皆为氢化物,三者皆为极性分子,其中A的相对分子质量最小;D、E、F皆为氧化物,且D、F皆为有毒气体.则:
①A、C、E三种氢化物沸点从高到低的顺序为
H2O>NH3>H2S
H2O>NH3>H2S
(填化学式);
②A和F在水溶液中充入O
2充分反应生成一种正盐,该反应的化学方程式为
2SO2+4NH3+2H2O+O2=2(NH4)2SO4
2SO2+4NH3+2H2O+O2=2(NH4)2SO4
(3)若B是由短周期元素组成的离子化合物,A、C为氧化物,E为气体单质,D、F是均有三种元素组成的离子化合物,它们的水溶液均呈碱性,相同浓度时D溶液的pH大于F.
①写出B的电子式
,
②B和C反应生成E和F的化学方程式
2Na2O2+2CO2=Na2CO3+O2
2Na2O2+2CO2=Na2CO3+O2
,列举该反应的一种用途
呼吸面具和潜水艇中做为氧气的来源
呼吸面具和潜水艇中做为氧气的来源
.

 A、B、C、D、E、F六种物质均是由短周期元素组成的中学常见的化学物质.它们之间的转化关系如下图.
A、B、C、D、E、F六种物质均是由短周期元素组成的中学常见的化学物质.它们之间的转化关系如下图.

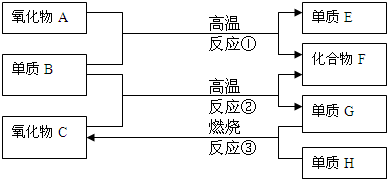
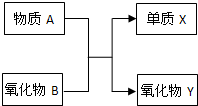 元素及其化合物的知识是“化学I”的重点内容. A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如图所示:
元素及其化合物的知识是“化学I”的重点内容. A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如图所示: