某研究性课题小组对氢氧化钠溶液和稀盐酸中和反应的有关问题,进行了如下探究:
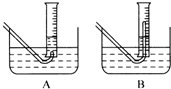
Ⅰ:(1)甲同学为了证明氢氧化钠溶液与稀盐酸能够发生反应,设计并完成了如下图所示实验.则X溶液是
酚酞
酚酞
.

(2)乙同学也设计完成了另一个实验,证明氢氧化钠溶液与盐酸能够发生反应.在盛有25.00mL稀盐酸的锥形瓶中,用胶头滴管慢慢滴入氢氧化钠溶液,不断振荡,每加一滴溶液测定并记录一次溶液的pH值,直至氢氧化钠溶液过量.
①写出测定溶液pH值的操作方法:
用干净的玻璃棒蘸取待测液点在pH试纸中间,将试纸的颜色与标准比色卡对照,读出溶液的pH
用干净的玻璃棒蘸取待测液点在pH试纸中间,将试纸的颜色与标准比色卡对照,读出溶液的pH
;
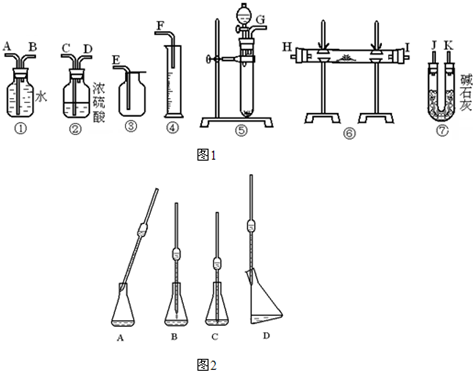
②下图中哪个图象符合该同学的记录
D
D
(填序号).

(3)你认为甲、乙两位同学的实验中,
乙同学
乙同学
(填“甲同学”、“乙同学”、“甲乙两同学”)的实验能充分证明氢氧化钠溶液与盐酸发生了反应,请说明理由:
甲同学的实验有可能是酚酞遇氢氧化钠溶液直接变成红色,乙同学的实验,随着滴加氢氧化钠溶液,溶液的pH由小于7逐渐增大到7,这充分证明溶液中的盐酸因反应而消耗了
甲同学的实验有可能是酚酞遇氢氧化钠溶液直接变成红色,乙同学的实验,随着滴加氢氧化钠溶液,溶液的pH由小于7逐渐增大到7,这充分证明溶液中的盐酸因反应而消耗了
.
Ⅱ:丙学生用0.100mol?L
-1氢氧化钠溶液滴定未知浓度的盐酸.他用移液管准确移取.
25.00mL未知浓度的盐酸置于一洁净的锥形瓶中,然后用0.100mol?L
-1的氢氧化钠溶液(指示剂为酚酞)进行滴定.滴定结果如下:
滴定次数 |
盐酸的体积/mL |
NaOH溶液的体积/mL |
| 滴定前刻度/mL |
滴定后刻度/mL |
| 1 |
25.00 |
2.00 |
20.20 |
| 2 |
25.00 |
1.02 |
21.03 |
| 3 |
25.00 |
0.20 |
20.20 |
(1)根据以上数据计算出盐酸的物质的量浓度为
0.080
0.080
mol?L
-1.
(2)如果滴定的终点没有控制好,即NaOH溶液过量,溶液显深红色,如何补救?请设计实验方案.
用上述未知浓度的盐酸进行反滴,记录所需盐酸的体积
用上述未知浓度的盐酸进行反滴,记录所需盐酸的体积
.