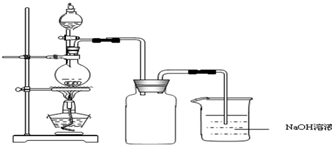
硫酸铜是一种应用极其广泛的化工原料.铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图所示).
(1)写出烧瓶中发生反应的化学方程式为:
Cu+H2SO4+2HNO3=CuSO4+2NO2↑+2H2O
或3Cu+3H2SO4+2HNO3=3CuSO4+2NO↑+4H2O
Cu+H2SO4+2HNO3=CuSO4+2NO2↑+2H2O
或3Cu+3H2SO4+2HNO3=3CuSO4+2NO↑+4H2O
.
(2)为符合绿色化学的要求,某研究性学习小组进行如下设计:
第一组:以空气为氧化剂法
方案1:以空气为氧化剂.将铜粉在仪器B中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应.
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应.向反应液中加FeSO
4或Fe
2(SO
4)
3,即发生反应.反应完全后向其中加物质甲调节pH 3~4,产生Fe(OH)
3沉淀,过滤、浓缩、结晶,滤渣作催化剂循环使用.已知:
| 沉淀物 |
Fe(OH)3 |
Cu(OH)2 |
Fe(OH)2 |
开始沉淀pH |
2.7 |
4.8 |
7.6 |
完全沉淀pH |
3.7 |
6.4 |
9.6 |
请回答下列问题:
①方案1中的B仪器名称是
坩埚
坩埚
.
②方案2中甲物质是
C
C
,最后所得晶体中可能含有
F
F
(填字母序号)
A、CaO B、NaOH C、CuCO
3 D、FeSO
4 E、Fe
2(SO
4)
3 F、FeSO
4?7H
2O
第二组:过氧化氢为氧化剂法
将3.2g铜丝放到45mL 1.5mol?L
-1的稀硫酸中,控温在50℃.加入18mL 10%的H
2O
2,反应0.5h后,升温到60℃,持续反应1h后,过滤、蒸发浓缩、减压抽滤等,用少量95%的酒精淋洗后晾干,得CuSO
4?5H
2O 10.5g.
请回答下列问题:
③加热时温度不宜过高的原因是
防止双氧水分解
防止双氧水分解
,写出组装减压抽滤装置的注意点
滤纸不得大于布氏漏斗底且覆盖所有小孔;橡皮塞插入部分不超过三分之二;布氏漏斗颈口斜面与吸滤瓶支管口相对;安全瓶中导管与吸滤瓶相连短与抽滤泵相连长
滤纸不得大于布氏漏斗底且覆盖所有小孔;橡皮塞插入部分不超过三分之二;布氏漏斗颈口斜面与吸滤瓶支管口相对;安全瓶中导管与吸滤瓶相连短与抽滤泵相连长
.(至少二点)
④本实验CuSO
4?5H
2O的产率为
84%
84%
.
上述两种氧化法中,更符合绿色化学理念的
第二组
第二组
(填“第一组”或“第二组”),理由是
第一组方案1需要灼烧,多消耗能源
第一组方案1需要灼烧,多消耗能源
.

 硫酸铜是一种应用极其广泛的化工原料.铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图所示).
硫酸铜是一种应用极其广泛的化工原料.铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图所示).