
题目列表(包括答案和解析)
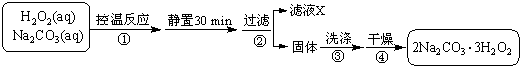
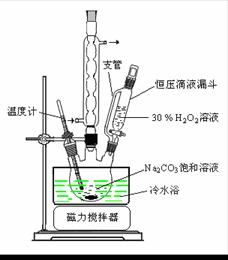
过碳酸钠(2Na2CO3·3H2O2)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂。某兴趣小组制备过碳酸钠的实验方案和装置示意图如下:
 已知:主反应 2Na2CO3 (aq) + 3H2O2 (aq)
已知:主反应 2Na2CO3 (aq) + 3H2O2 (aq) ![]() 2Na2CO3·3H2O2 (s) ΔH < 0
2Na2CO3·3H2O2 (s) ΔH < 0
副反应 2H2O2 = 2H2O + O2↑
滴定反应 6KMnO4 + 5(2Na2CO3·3H2O2) +19H2SO4 =
3K2SO4 + 6MnSO4 +10Na2SO4 + 10CO2 ↑ + 15O2↑ + 34H2O
50 °C时 2Na2CO3·3H2O2 (s) 开始分解
请回答下列问题:
(1)图中支管的作用是 。
(2)步骤①的关键是控制温度,其措施有 、 和 。
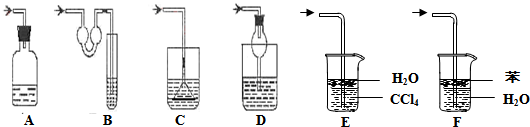
(3)在滤液X中加入适量NaCl固体或无水乙醇, 均可析出过碳酸钠,原因是 。
(4)步骤③中选用无水乙醇洗涤产品的目的是 。
(5)下列物质中,会引起过碳酸钠分解的有 。
A.Fe2O3 B.CuO
C.Na2SiO3 D.MgSO4
(6)准确称取0.2000 g 过碳酸钠于250 mL 锥形瓶中,加50 mL 蒸馏水溶解,再加50 mL 2.0 mol·L-1 H2SO4,用2.000×10-2 mol·L-1 KMnO4 标准溶液滴定至终点时消耗30.00 mL,则产品中H2O2的质量分数为 。
 ④取下锥形瓶,滴加指示剂,用0.1000mol?L-1盐酸标准液滴定;
④取下锥形瓶,滴加指示剂,用0.1000mol?L-1盐酸标准液滴定;| 实验编号 | 样品和辅助试剂 | 消耗盐酸体积(mL) |
| 1 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.45 |
| 2 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.55 |
| 3 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.50 |
| 4 | 10.00mL蒸馏水、0.2g催化剂、20mL浓硫酸 | 1.50 |
(18分)Ⅰ测定水中溶解氧的方法是:在水中加入硫酸锰及氢氧化钠和碘化钾溶液,生成氢氧化锰沉淀。氢氧化锰性质极不稳定,迅速与水中溶解氧化合生成锰酸锰:
2MnSO4+4NaOH=2Mn(OH)2↓+2Na2SO4--------------①
2Mn(OH)2+O2=2H2MnO3---------------------------②
H2MnO3十Mn(OH)2=MnMnO3↓+2H2O------③
加入硫酸溶液,使沉淀(MnMnO3)与溶液中所加入的碘化钾发生反应,
2KI+H2SO4=2HI+K2SO4--------------------------- --------④
MnMnO3+2H2SO4+2HI=2MnSO4+I2+3H2O ----—⑤
用已知浓度的Na2S2O3溶液滴定生成的碘,根据消耗的Na2S2O3的体积可以测定水中溶氧量(mg/L)
I2+2Na2S2O3=2NaI+Na2S4O6
测定中,用移液管取50.00 mL水样,迅速加入预先配置好的MnSO4和NaOH混合溶液,再加入KI溶液,立即塞好塞子,震荡使反应完全。打开塞子,迅速加入适量的稀硫酸,期间发生①—⑤反应生成单质碘。用0.10mol/LNa2S2O3溶液滴定生成的碘,消耗了2.68mL Na2S2O3溶液。
已知:H2S2O3 为弱酸
回答下列问题:
(1)盛放Na2S2O3溶液的滴定管种类为
(2)该滴定的指示剂为 ,滴定时,溶液由 色到 色,且半分钟内颜色不再变化即达到滴定终点
(3)下列操作和该滴定有关并会导致测定水中溶氧偏高的是( )
A滴定前滴定管尖嘴无气泡,滴定结束尖嘴有气泡 B锥形瓶用待装液润洗
C滴定管读数开始平视,滴定结束时立即平视读数 D酸式滴定管没有用待装液润洗
(4)水中溶氧量为 mg/L水。
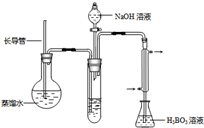
Ⅱ50.00mL0.50mol/L盐酸跟50.0mL0.55mol/L氢氧化钠溶液在下图装置中进行中和反应,通过测定反应前盐酸和氢氧化钠溶液各自的温度和中和过程中混合液的最高温度可计算中和热.试回答下列问题.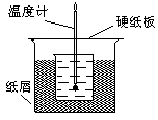
(1)该实验装置设计中缺少的仪器的名称为
(2)若实验测得放出热量为1.43kJ,写出表示中和热的热化学方程式
(3)改用60.0mL0.5mol/L盐酸跟50.0mL0.55mol/L氢氧化钠溶液进行反应,与上述实验相比,所放热量 等,所求中和热数值 等。(填“相等,不相等”)
(15分)随着信息产业的高速发展和家用电器的普及,我国印刷电路板(PCB)的生产呈现急剧增长之势。废旧电路板的增多给我们带来了环境问题,目前我们台州大多采用32%~35%的FeCl3溶液溶解印刷线路板上的金属铜,从而进行对铜的回收和利用。经分析腐蚀废液中主要含有HCl 、FeCl2和CuCl2等溶质。
(1)用32%~35%的FeCl3溶液溶解印刷线路板上的金属铜的原理是
(用离子方程式表示): ▲ 。
(2)工业上有多种回收腐蚀废液中铜的方法,下面是常用的两种方法:
Ⅰ、电化学方法回收腐蚀废液中铜,则阳极(石墨)上的电极反应式为: ▲ 。
Ⅱ、工业上也可以用铁粉回收腐蚀废液中的铜:
①用铁粉回收铜的实验操作为 ▲ 。
②科学家对铁置换铜工艺的研究如下:
分别用还原铁粉、废铁屑和废铁屑在超声波粉碎处理下置换铜,将置换出的铜粉放入250mL烧杯中,加入120mL 1.5 mol·L-1的硫酸,水浴加热,控制温度在70 ℃,搅拌,在10、20、30、40、50、60min时,分别用吸管移取0.5g左右的铜于试管内,将上层清液倒回小烧杯中,用蒸馏水洗净试样,过滤,在105℃烘箱中烘干后测定铜粉中铁的含量。其结果如图所示。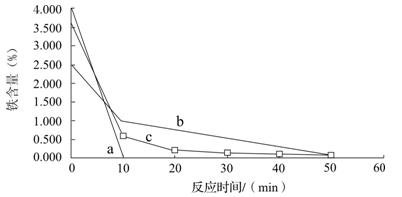
已知a表示用还原铁粉置换铜的除铁效果,b表示用废铁屑置换铜的除铁效果,c表示用废铁屑在超声波下置换铜的除铁效果,你认为除铁效果最好的是 ▲ (填a、b或c),其原因是 ▲ 。
(3)工业上也可用腐蚀废液生成CuCl2·2H2O,从而进行对废液的利用,其工艺流程如下:
已知:pH ≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH ≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀。
①试剂A最好应选用 ▲ 。
a.浓硫酸 b.Cl2 c.NaClO d.NaOH溶液
理由是 ▲ 。
②分析有关物质的溶解度曲线(如下图),为了获得CuCl2·2H2O晶体,对滤液B进行的操作是: ▲ 、 ▲ ,过滤得到产品。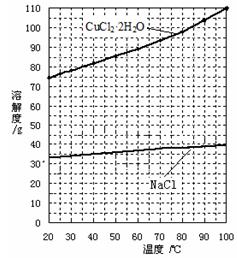
③测定CuCl2·2H2O产品的质量分数可按下法:取2.000g产品,用水溶解后,加入60.00 mL 0.4000 mol·L-1的KI溶液(足量),充分反应后加入淀粉指示剂,用0.4000 mol·L-1 Na2S2O3标准溶液滴定,耗去此标准液25.00 mL时,刚好到达滴定终点。
已知:2Cu2++4I-=2CuI↓+I2 I2+2S2O32-=2I-+S4O62-
此产品中CuCl2·2H2O的质量分数为 ▲ 。
某化学研究性学习小组拟测定食醋的总酸量(g/100 mL),请你参与该小组的实验并回答相关问题。
[实验目的]测定食醋的总酸量
[实验原理]中和滴定
[实验用品]蒸馏水,市售食用白醋样品500 mL(商标注明总酸量:3.50 g/100 mL~5.00 g/100 mL),0.1000 mol/L NaOH标准溶液;100 mL容量瓶,10 mL移液管,碱式滴定管,铁架台,滴定管夹,锥形瓶,烧杯,酸碱指示剂(可供选用的有:甲基橙、酚酞、石蕊)。
[实验步骤]①配制并移取待测食醋溶液
用10 mL移液管吸取10.00 mL市售白醋样品置于100 mL容量瓶中,用处理过的蒸馏水稀释至刻度线,摇匀后用酸式滴定管取待测食醋溶液20.00 mL,并移至锥形瓶中。
②盛装标准NaOH溶液
将碱式滴定管洗净后,用NaOH标准溶液润洗3次,然后加入NaOH标准溶液,排除尖嘴部分气泡后,使液面位于“0”刻度或“0”刻度以下。静置,读取数据并记录为NaOH标准溶液体积的初读数。
③滴定
往盛有待测食醋溶液的锥形瓶中滴加某酸碱指示剂1~2滴,滴定至终点。记录NaOH的终读数。重复滴定3次。
[数据记录]
|
滴定次数 实验数据 |
1 |
2 |
3 |
4 |
|
V(样品)/mL |
20.00 |
20.00 |
20.00 |
20.00 |
|
V(NaOH)始/mL |
0.00 |
0.20 |
0.10 |
0.10 |
|
V(NaOH)终/mL |
14.98 |
15.20 |
15.12 |
16.24 |
[问题与思考]
(1)步骤①中还需补充的仪器有
________________________________________________________________________,
蒸馏水的处理方法是
________________________________________________________________________。
(2)步骤③中你选择的酸碱指示剂是
________________________________________________________________________,
理由是________________________________________________________________________
________________________________________________________________________。
(3)若用深色食醋进行实验,为准确判断滴定终点,可采取的措施是
________________________________________________________________________。
(4)样品总酸量约为________g/100 mL。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com