
题目列表(包括答案和解析)
(9分)用Na2CO3·10H2O晶体,配制0.2 mol/L的Na2CO3溶液480 mL。
(1)实验中用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少_____________,____________;
(2)应用托盘天平称取Na2CO3·10H2O的晶体的质量为_________________g;
(3)配制溶液时有以下几个操作:
①溶解 ②摇匀 ③洗涤 ④冷却 ⑤称量 ⑥转移溶液 ⑦定容
正确的操作顺序是__________________(填序号)。
(4)根据下列操作对所配溶液的浓度各有什么影响,完成填空。
①碳酸钠晶体失去了部分结晶水 ②用“左码右物”的称量方法称量晶体
③碳酸钠晶体不纯,其中混有氯化钠 ④称量碳酸钠晶体时所用砝码生锈
⑤容量瓶未经干燥就使用
其中引起所配溶液浓度偏高的有____________,无影响的有________。(填序号)
用Na2CO3·10H2O晶体,配制0.2 mol/L的Na2CO3溶液480 mL。
(1)实验中用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少_____________, _______ ____;
(2)应用托盘天平称取Na2CO3·10H2O的晶体的质量为_________________g;
(3)配制溶液时有以下几个操作:
①溶解 ②摇匀 ③洗涤 ④冷却 ⑤称量 ⑥转移溶液 ⑦定容
正确的操作顺序是__________________(填序号)。
(4)根据下列操作对所配溶液的浓度各有什么影响,完成填空。
①碳酸钠失去了部分结晶水 ②用“左码右物”的称量方法称量晶体
③碳酸钠晶体不纯,其中混有氯化钠 ④称量碳酸钠晶体时所用砝码生锈
⑤容量瓶未经干燥就使用
其中引起所配溶液浓度偏高的有____________,无影响的有________。(填序号)
(12分)用Na2CO3·10H2O晶体,配制0.2 mol/L的Na2CO3溶液480 mL。
(1)实验中用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少_____________,____________;
(2)应用托盘天平称取Na2CO3·10H2O的晶体的质量为_________________g;
(3)配制溶液时有以下几个操作:①溶解 ②摇匀 ③洗涤并转移洗涤液 ④冷却 ⑤称量 ⑥转移溶液 ⑦定容
正确的操作顺序是__________________(填序号)。
(4)根据下列操作对所配溶液的浓度各有什么影响,完成填空。
①碳酸钠失去了部分结晶水 ②用“左码右物”的称量方法称量晶体
③碳酸钠晶体不纯,其中混有氯化钠 ④称量碳酸钠晶体时所用砝码生锈
⑤容量瓶未经干燥就使用
其中引起所配溶液浓度偏高的有_________,无影响的有________。(填序号)
(1)现需要配制500 mL 1 mol·L-1硫酸溶液,需用质量分数为98%、密度为1.84 g·cm-3的浓硫酸 ________mL。
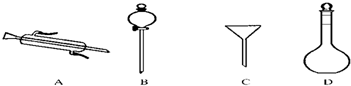
(2)从上述仪器中,按实验使用的先后顺序,其编号排列是___________________。
(3)容量瓶使用前检验漏水的方法是___________。
(4)若实验遇到下列情况,对硫酸溶液的物质的量浓度有何影响(填写“偏高”“偏低”或“不变”)?
①用以稀释硫酸的烧杯未洗涤,_________________________________。
②未经冷却趁热将溶液注入容量瓶中,___________________________。
③摇匀后发现液面低于刻度线再加水,___________________________。
④容量瓶中原有少量蒸馏水,___________________________________。
⑤定容时观察液面俯视,_______________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com