
题目列表(包括答案和解析)




| ||
| ||
| ||
| ||
 HSiO3-+OH-、HSiO3-+H2O
HSiO3-+OH-、HSiO3-+H2O H2SiO3+OH-、AlO2-+2H2O
H2SiO3+OH-、AlO2-+2H2O Al(OH)3+OH-,降低pH有利于水解平衡向正反应方向移动,当pH调到7~8时能使它们完全水解生成沉淀
Al(OH)3+OH-,降低pH有利于水解平衡向正反应方向移动,当pH调到7~8时能使它们完全水解生成沉淀 HSiO3-+OH-、HSiO3-+H2O
HSiO3-+OH-、HSiO3-+H2O H2SiO3+OH-、AlO2-+2H2O
H2SiO3+OH-、AlO2-+2H2O Al(OH)3+OH-,降低pH有利于水解平衡向正反应方向移动,当pH调到7~8时能使它们完全水解生成沉淀
Al(OH)3+OH-,降低pH有利于水解平衡向正反应方向移动,当pH调到7~8时能使它们完全水解生成沉淀| 294×c×V×V2 |
| 6×1000×V1×m |
| 294×c×V×V2 |
| 6×1000×V1×m |
过碳酸钠(Na2CO4)在洗涤、印染、造纸、医药卫生等领域有大量应用.
已知:过碳酸钠与硫酸溶液反应的化学方程式如下:
Na2CO4+H2SO4→Na2SO4+H2O2+CO2↑ 2H2O2→2H2O+O2↑
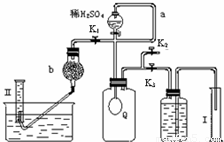
为测定已变质的过碳酸钠(含碳酸钠)的纯度,设计如图所示的实验:Q为-具有良好的弹性的气球(不与反应物和生成物反应),称取一定量的样品和少量二氧化锰放于其中,按图安装好实验装置,打开分液漏斗的活塞,将稀H2SO4滴入气球中.

(1)Q内发生反应生成的气体为_________,导管a作用是_________.
(2)为测出反应时生成气体的总体积,滴稀H2SO4前必须关闭K1、K2,打开K3.当上述反应停止,将K1、K2、K3处于关闭状态,然后先打开K2,再缓缓打开K1,这时可观察到的现象是_________,b中装的碱石灰的作用是_________.
(3)实验结束时,量筒I中有x mL水,量筒Ⅱ中收集到y mL气体(上述体积均已折算到标准状况),则过碳酸钠的纯度是_________
(4)某同学实验测得的过碳酸钠的纯度超过100%,你认为可能的原因是_________
A.气体滞留在Q和导气管中,未全部进入量筒Ⅱ
B.量筒Ⅱ读数时,量筒液面高于水槽液面
C.右侧量筒Ⅰ和储液集气瓶连接导管内的液体没有计入读数x
D.气体体积数值x、y没有扣除滴加的硫酸的体积
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com