
题目列表(包括答案和解析)
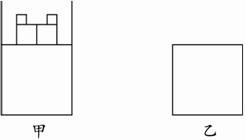
 在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物.该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉.现用下图中甲、乙两套仪器装置制取上述铁的氧化物和细铁粉.制取上述铁的氧化物和细铁粉时必须使用普通铁粉和6mol?L-1盐酸,其他试剂任选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热装置等以及仪器中所装的试剂在图中均已略去).
在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物.该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉.现用下图中甲、乙两套仪器装置制取上述铁的氧化物和细铁粉.制取上述铁的氧化物和细铁粉时必须使用普通铁粉和6mol?L-1盐酸,其他试剂任选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热装置等以及仪器中所装的试剂在图中均已略去).
| ||
| ||


(1)甲容器达平衡状态时SO2的转化率_____________________________。
(2)甲容器达到平衡所需的时间________________乙容器达到平衡所需时间(填“大于”“小于”或“等于”);反应过程中放出的能量,甲_______________乙(填“大于”“小于”或“等于”),其原因是____________________________________________________________。
(3)甲、乙两容器达到平衡状态后,若要使甲、乙两容器中SO2浓度相等,可以采取的措施是:________________________________________。
A.保持温度不变,适当扩大甲容器的体积?
B.保持容器体积不变,使容器乙升温?
C.保持容器的体积和温度不变,向乙容器加入适量的SO3??
D.保持容器的体积和温度不变,向甲容器加入适量的SO3??
(4)若起始时,甲容器加入a mol SO2、b mol O2和c mol SO3,保持温度不变,达到平衡时,混合气体中各气体的体积分数与题干中甲容器相同。则a、b、c应满足的条件是:________________________________________________。
将有机化合物的分子式或结构简式变形书写,在分析问题的过程会取得意想不到的好效果。已知甲酸(HCOOH)与浓硫酸混合在50——60℃时,会发生脱水生成CO;乙醇(CH3CH2OH)与浓硫酸混合在170℃时脱水生成乙烯(C2H4或CH2=CH2),则草酸HOOC—COOH与浓硫酸在一定温度下脱水会生成
A、CO B、CO2 C、CO和 CO2 D、C2O3
将有机化合物的分子式或结构简式变形书写,在分析问题的过程会取得意想不到的好效果。已知甲酸(HCOOH)与浓硫酸混合在50——60℃时,会发生脱水生成CO;乙醇(CH3CH2OH)与浓硫酸混合在170℃时脱水生成乙烯(C2H4或CH2=CH2),则草酸HOOC—COOH与浓硫酸在一定温度下脱水会生成
| A.CO | B.CO2 | C.CO和 CO2 | D.C2O3 |
铜及其化合物在生产生活中有广泛应用,铜在化合物中的常见化合价有+l、+2。已知Cu2O与稀硫酸反应,溶液呈蓝色。
(1)工业上可用Cu2S+O2 2Cu+SO2反应制取粗铜,当有32gCu2S消耗时,电子转移数目是
。
2Cu+SO2反应制取粗铜,当有32gCu2S消耗时,电子转移数目是
。
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入H2O2,反应一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,温度控制在50℃-60℃的两个原因除了加快反应速率外,还有 。在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液加热,生成CuCl沉淀,写出生成CuCl的离子方程式 。
(3)某小组同学在做铜与浓硫酸反应的实验时,发现铜片表面有黑色固体生成。
①甲同学猜想:黑色固体是未来得及溶解于酸的CuO, 其猜想可用化学方程式表示为:
Cu + H2SO4
②乙同学认为:黑色固体除CuO外还可能含有Cu2S和CuS.其理由可能是 (填字母)
a.Cu2S和CuS都是黑色的
b.铜与浓硫酸在加热条件下反应,还可能放出O2
c.浓硫酸是氧化剂,铜是还原剂,Cu的化合价上升与S的化合价下降有多种可能
(4)现向Cu、Cu2O和CuO组成的混合物中,加入1 L 0.6 mol/L HNO3溶液恰好使混合物溶解,同时收集到2240 mL NO气体(标准状况)。Cu2O跟稀硝酸反应的离子方程式 。若将上述混合物用足量的H2加热还原,所得到固体的质量为 g。若混合物中含0.1 mol Cu,将该混合物与稀硫酸充分反应,至少消耗H2SO4的物质的量为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com