
题目列表(包括答案和解析)
(9分)红磷P(s)和Cl2 (g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示
(图中的ΔH表示生成lmol产物的数据)。
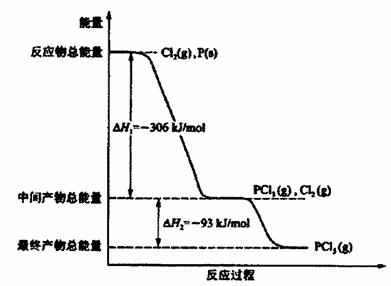
根据上图回答下列问题:
(1) PCl5分解成PCl3 和Cl2的热化学方程式是________ ______;
上述分解反应是一个可逆反应。温度T1时,在密闭容器中加人0.80 mol PC15,反应达平衡时PC15还剩0.60 mol,其分解率α1等于________;若反应温度由Tl升高到T2,平衡时PC15的分解率α2为,α2_______α1(填“大于”、“小于”或“等于”) ;
(2)工业上制备PCl5通常分两步进行,先将P和Cl2反应生成中间产物PCl3,然后降温,再和Cl2反应生成PCl5原因是_______________________________________________
(3)P和Cl2分两步反应生成1molPCl5的ΔH3 =_____________________,P和Cl2一步反应生成1 mol PCl5的ΔH4___________ΔH3;(填“大于”、“小于”或“等于”)
(9分)红磷P(s)和Cl2 (g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示
(图中的ΔH表示生成lmol产物的数据)。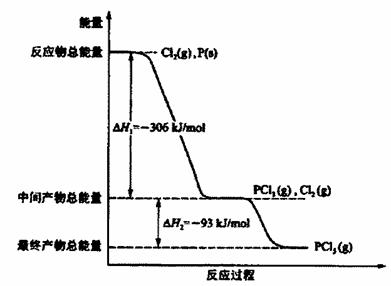
根据上图回答下列问题:
(1) PCl5分解成PCl3 和Cl2的热化学方程式是________ ______;
上述分解反应是一个可逆反应。温度T1时,在密闭容器中加人0.80 mol PC15,反应达平衡时PC15还剩0.60 mol,其分解率α1等于________;若反应温度由Tl升高到T2,平衡时PC15的分解率α2为,α2_______α1(填“大于”、“小于”或“等于”) ;
(2)工业上制备PCl5通常分两步进行,先将P和Cl2反应生成中间产物PCl3,然后降温,再和Cl2反应生成PCl5原因是_______________________________________________
(3)P和Cl2分两步反应生成1molPCl5的ΔH3 =_____________________,P和Cl2一步反应生成1 mol PCl5的ΔH4___________ΔH3;(填“大于”、“小于”或“等于”)
多硫化物S![]() (x=2~6),在碱性溶液中被BrO
(x=2~6),在碱性溶液中被BrO![]() 氧化成SO
氧化成SO![]() ,而BrO
,而BrO![]() 被氧化成SO
被氧化成SO![]() ,而BrO
,而BrO![]() 被还原成Br-。在反应中BrO
被还原成Br-。在反应中BrO![]() 和OH-的物质的量之比为2∶3,则x值为________,其反应的离子方程式为____
____
和OH-的物质的量之比为2∶3,则x值为________,其反应的离子方程式为____
____
|
温度 实验次数 |
起始温度t1/℃ |
终止温度 t2/℃ |
温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | 4.0 4.0 |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com