
题目列表(包括答案和解析)
有关物质的转化关系如下图所示(部分物质和条件已略去)。B、C、E是常见气体;A、X、Y是常见金属单质,其中Y既能与强酸反应,又能与强碱反应;G的焰色反应显黄色;I的溶液滴加KSCN显血红色。
请回答下列问题:
(1)F的化学式为 。
(2)I的化学式为 。
(3)写出Y和D溶液反应的离子方程式: 。
(4)写出C与H溶液反应的化学方程式,并用双线桥标出电子转移的方向和数目: 。
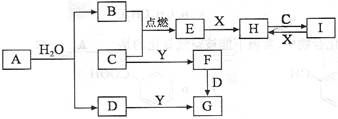
有关物质的转化关系如下图所示(部分物质和条件已略去)。B、C、E是常见气体;A、X、Y是常见金属单质,其中Y既能与强酸反应,又能与强碱反应;G的焰色反应显黄色;I的溶液滴加KSCN显血红色。
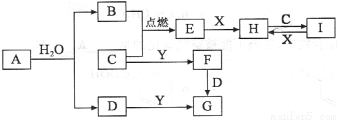
请回答下列问题:
(1)F的化学式为 。
(2)I的化学式为 。
(3)写出Y和D溶液反应的离子方程式: 。
(4)写出C与H溶液反应的化学方程式,并用双线桥标出电子转移的方向和数目: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com