
题目列表(包括答案和解析)

图1-3-19
其中A和G的摩尔质量相等,且A为含非极性键的离子化合物;B在常温下是液态化合物;D是双原子气体单质;H是常见金属。
(1)A的电子式:___________。
(2)H和C溶液反应的化学方程式为___________。其中氧化剂是___________。
(3)用离子方程式表示E的水溶液呈碱性的原因___________。
(4)在E溶液转化为G的⑤反应中,最好选用下列哪种试剂___________,其理由是_____________________________________________________________________。
A.稀盐酸 B.CO2 C.氨水 D.NaOH溶液 E.H2O
(5)若H与金属镁用导线连接后插入C溶液中可以构成原电池,写出负极的电极反应式:___________。
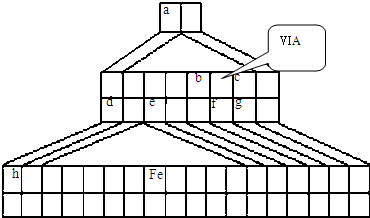
a,b,c,d,e,f,g,h为8种由短周期元素构成的微粒,它们都有10个电子,其结构特点如下:

其中b离子半径大于e离子半径;d由4原子构成;c与f可形成2个g分子,d与h在一定条件下可相互转化,试写出:
(1)a微粒原子核外结构示意图________.
(2)b与e相应元素最高价氧化物对应水化物的碱性强弱为:________>________(写化学式).
(3)大量c微粒和大量h微粒共热生成d微粒的离子方程式________.
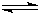 NH3?H2O+H+
NH3?H2O+H+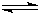 NH3?H2O+H+
NH3?H2O+H+

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com