
二甲醚(CH
3OCH
3)具有优良的燃烧性能,被称为21世纪的“清洁能源”.一步法合成二甲醚是以合成气(CO/H
2)为原料,在一定温度、压强和催化剂作用下进行,反应器中发生了下列反应:
①CO(g)+2H
2(g )?CH
3OH(g);△H
1=90.7 kJ?mol
-1②2CH
3OH(g)?CH
3OCH
3(g)+H
2O(g);△H
2=23.5 kJ?mol
-1③CO(g)+H
2O?(g)CO
2(g)+H
2(g);△H
3=41.2 kJ?mol
-1(1)-步法合成二甲醚的总反应可表示为3CO(g)+3H
2(g)CH
3OCH
3(g)+CO
2(g),该反应的AH=
-246.1kJ/mol
-246.1kJ/mol
.平衡常数表达式为
K=
| c(CH3OCH3)?c(CO2) |
| c3(CO)?c3(H2) |
K=
| c(CH3OCH3)?c(CO2) |
| c3(CO)?c3(H2) |
.
(2)另一种合成二甲醚的方法称为“二步法”,该工艺为让反应①和反应②分别在不同的反应器中进行,无反应③发生,而“一步法”的反应③的发生提高了CH
3OCH
3的产率,原因是
反应③消耗了反应②中的水,使得②的平衡正向移动,从而提高了甲醚的产率
反应③消耗了反应②中的水,使得②的平衡正向移动,从而提高了甲醚的产率
.
(3)由CO
2加氢直接合成二甲醚可以消除过度CO
2排放对环境的影响.当在合成反应器中加入碳氢比[n(CO
2)/n(H
2)]为1:3的混合气体,在一定条件下反应得到二甲醚和水蒸气,实现了CO
2的减排目的.该反应的反应方程式为
; 判断该反应在一定温度下,体积恒定的密闭容器中下列不能作为达到化学平衡状态的依据是
A
A
A.容器的密度不变
B.容器内压强保持不变
C,平均摩尔质量保持不变
D.单位时间内消耗2mol CO
2,同时消耗1mol二甲醚
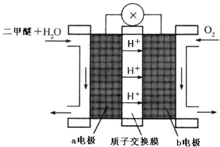
(4)以二甲醚为燃料的燃料电池工作原理如图所示:则正极为
B
B
(填A极或B极),写出A电极反应式
CH3OCH3+3H2O-12e-=2CO2+12H+
CH3OCH3+3H2O-12e-=2CO2+12H+
.


 二甲醚(CH3OCH3)具有优良的燃烧性能,被称为21世纪的“清洁能源”.一步法合成二甲醚是以合成气(CO/H2)为原料,在一定温度、压强和催化剂作用下进行,反应器中发生了下列反应:
二甲醚(CH3OCH3)具有优良的燃烧性能,被称为21世纪的“清洁能源”.一步法合成二甲醚是以合成气(CO/H2)为原料,在一定温度、压强和催化剂作用下进行,反应器中发生了下列反应: