
题目列表(包括答案和解析)
下图为将Zn投入一定浓度体积的H2SO4中,解释图像的成因(纵坐标为H2的生成速率)
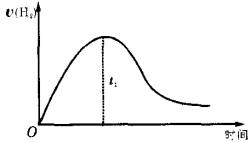

(1)0—t1速率变化的原因是______________________________。
(2)t1—t2速率变化的原因是______________________________。
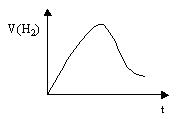 将Zn投入一定浓度一定体积的盐酸中,H2的生成速率与时间的关系如图所示,试解释图中曲线变化的原因(纵坐标为H2的生成速率,横坐标为时间)。
将Zn投入一定浓度一定体积的盐酸中,H2的生成速率与时间的关系如图所示,试解释图中曲线变化的原因(纵坐标为H2的生成速率,横坐标为时间)。
答:① ;
② 。
下图所示为将Zn投入一定浓度一定体积的H2SO4溶液中,解释图象的成因(纵坐标为H2的生成速率).
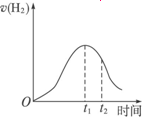
(1)0-t1速率变化的原因是________.
(2)t1-t2速率变化的原因是________.
A.504 mL B.336 mL C.224 mL D.168 mL
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com