化学实验室通常用粗锌和稀硫酸反应制氢气,因此在制氢废液中含有大量的硫酸锌.同时,由于粗锌中还含有铁等杂质,使得溶液中混有一定量的硫酸亚铁,为了充分利用制氢废液,常用其制备皓矾(ZnSO
4?7H
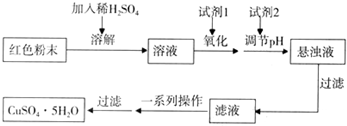
2O).某校化学兴趣小组的同学以制氢气的废液为原料来制取皓矾.制备皓矾的实验流程如图所示.

已知:开始生成氢氧化物沉淀到沉淀完全的pH范围分别为:Fe(OH)
3:2.7-3.7Fe(OH)
2:7.6-9.6 Zn(OH)
2:5.7-8.0试回答下列问题:?
(1)加入的试剂①,供选择使用的有:氨水、NaClO溶液、20%的H
2O
2、浓硫酸、浓硝酸等,最好选用
20%的H2O2
20%的H2O2
,其理由是
将制氢废液中的Fe2+氧化成Fe3+,同时避免引入新的杂质
将制氢废液中的Fe2+氧化成Fe3+,同时避免引入新的杂质
;
(2)加入的试剂②,供选择使用的有:a、Zn粉,b、ZnO,c、Zn(OH)
2,d、ZnCO
3,e、ZnSO
4等,可选用
bcd
bcd
;
(3)从晶体1→晶体2,该过程的名称是
重结晶
重结晶
;
(4)在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是
为了冲洗掉晶体表面的杂质离子;防止晶体溶解,影响产率
为了冲洗掉晶体表面的杂质离子;防止晶体溶解,影响产率
.



 2C(g)
2C(g)  X(g)+Y(g)
X(g)+Y(g)

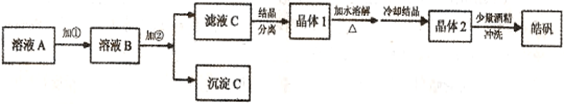 (l)制备皓矾的实验流程如下图所示。
(l)制备皓矾的实验流程如下图所示。