
题目列表(包括答案和解析)
当化学反应:![]()
![]()
![]() 处于平衡状态时,向其中加入一种
处于平衡状态时,向其中加入一种![]() 含量较多的氯气,平衡发生移动,在建立新平衡以前,
含量较多的氯气,平衡发生移动,在建立新平衡以前,![]() 中所含
中所含![]() 的百分含量比原平衡状态时是否会增加?请说明理由.
的百分含量比原平衡状态时是否会增加?请说明理由.
当化学反应 (g)
(g)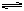
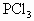 (g)+
(g)+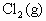 处于平衡状态时,向其中加入一种
处于平衡状态时,向其中加入一种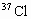 含量较多的氯气,平衡发生移动,在建立新平衡以前,
含量较多的氯气,平衡发生移动,在建立新平衡以前,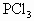 中所含
中所含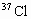 的百分含量比原平衡状态时是否会增加?请简述理由.
的百分含量比原平衡状态时是否会增加?请简述理由.
当化学反应PCl5(g)![]() PCl3(g)+Cl2(g)处于平衡状态时,向其中加入一种37Cl含量较多的氯气,平衡发生移动。在建立新平衡以前,PCl3中所含37Cl的质量分数比原平衡状态时(填“增加”或“减少”)___________,理由是___________________________。
PCl3(g)+Cl2(g)处于平衡状态时,向其中加入一种37Cl含量较多的氯气,平衡发生移动。在建立新平衡以前,PCl3中所含37Cl的质量分数比原平衡状态时(填“增加”或“减少”)___________,理由是___________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com