
题目列表(包括答案和解析)
(1)写出硝酸跟银反应制取硝酸银的化学方程式,说明选用稀硝酸跟银反应制取硝酸银的主要原因。
(2)当银与稀硝酸的反应完毕后,要加入少量银屑并保温,调整溶液的pH为4后,在所得溶液中,通入过热水蒸气,过滤后,把滤液蒸发、冷却,得到硝酸银晶体。简析上述操作的化学原理。
(3)该反应放出的尾气不能直接向大气排放,而应当在吸收塔中用氢氧化钠溶液进行吸收,简述其主要目的。
工业上由银与硝酸反应来制取硝酸银.在实际生产中,先要把购进的浓硝酸加入等体积水稀释后,再跟银反应,在加热条件下使反应完成.试简要回答以下各问:
(1)为什么不要浓硝酸直接跟银反应来制取硝酸银?
(2)当反应完毕为什么要调整溶液pH值为4后,通入过热水蒸气,过滤后,把滤液蒸发得到晶体硝酸银?
(3)该反应放出的尾气主要成分是什么?为什么要选用NaOH溶液吸收.
工业上由银与硝酸反应来制取硝酸银.在实际生产中,先要把购进的浓硝酸加入等体积水稀释后,再跟银屑在加热条件下使反应完成.试简要回答以下各问:
(1)在实际生产中,为什么不用浓硝酸直接跟银反应来制取硝酸银?
(2)当![]() 与
与![]() 反应完毕,为什么要调整溶液pH为4后,还需通入过热水蒸气?过滤后,将滤液蒸发,冷却析出硝酸银晶体的目的是什么?
反应完毕,为什么要调整溶液pH为4后,还需通入过热水蒸气?过滤后,将滤液蒸发,冷却析出硝酸银晶体的目的是什么?
(3)该反应产生的尾气主要成份是什么?对环境有何危害?应当怎样处理尾气?

(1)实验室制取氨气的化学方程式为 ,工业上合成氨采取的下列措施中可用勒夏特列原理解释的是? ?(填字母)?
A.采用较高压强(20 Mpa~50 Mpa)?
B.采用500 ℃的高温?
C.用铁触媒作催化剂?
D.将生成的氨液化并及时从体系中分离出来,N2和H2循环到合成塔中并补充N2和H2?
(2)适当改变如图所示的装置后,也可用来制取和收集氧气。改变的方法是: 。?
(3)实验室用浓硫酸和铜制取并收集少量的SO2气体,能否采用该装置 ? ?(填“能”或“不能”),若选填“能”,请说明理由;若选填“不能”,则怎样改变该装置后就能达到实验目的?请用文字说明 ;?
(4)取6.4 g铜片和12 mL 18.4 mol·L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,某同学根据所学的化学知识认为还有一定量的硫酸剩余。下列药品能够用来证明反应结束后烧瓶中确实有余酸的是?? ??(填字母)。?
A.铁粉 B.氯化钡溶液? C.银粉 D.碳酸氢钠溶液?
(5)为定量测定余酸物质的量浓度,某同学进行了如下设计:先测定铜片与浓硫酸反应产生SO2的量,再计算余酸的物质的量浓度。测定SO2的量的方案很多,下列方案可行的
是 (填字母)?
A.将装置中产生的气体缓缓通过预先称量过盛有碱石灰的干燥管,结束反应后再次称量?
B.将装置中产生的气体缓缓通入足量氢氧化钡溶液,反应完全后过滤、洗涤、干操、称量沉淀?
C.将装置中产生的气体缓缓通入足量硝酸酸化的硝酸钡溶液,反应完全后过滤、洗涤、干燥、称量沉淀?
请对不可行的方案进行分析(可以不填满)
方案序号 | 分析 | 误差(偏高或偏低) |
|
|
|
|
|
|
|
|
|
(6)请再设计其他可行的实验方案来测定余酸的物质的量浓度,简要写出操作步骤及需要测定的数据(不必计算)。??
氧化铁是重要工业颜料。工业上通常以废铁屑(杂质不与酸反应)为原料制备FeCO3,再将其煅烧制取氧化铁。工业制备FeCO3的流程如下:
回答下列问题:
(1)操作Ⅰ的名称是 。
(2)写出生成FeCO3沉淀的离子方程式 。
(3)有些同学认为滤液Ⅰ中铁元素含量可用KMnO4溶液来测定(5Fe2++MnO-4+8H+=5Fe3++Mn2++4H2O)。
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的玻璃仪器除玻璃棒、烧杯、胶头滴管外,还需 。
②某同学设计了下列滴定方式(夹持部分略去),最合理的是 。(填字母序号)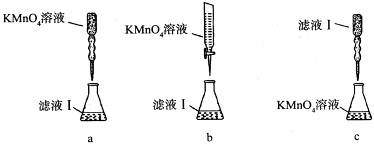
(4)该流程中用到的Na2CO3在工业生产中常含有少量NaCl。某校化学活动社团设计如图所示装置来测定Na2CO3的含量。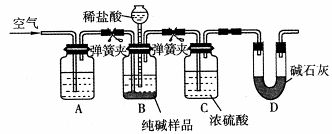
①要检验Na2CO3中杂质的存在,选用下列试剂中的 (选填序号)。
a.氢氧化钡溶液 b.稀硝酸 c.硫氰酸钾溶液 d.硝酸银溶液
②检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后静置,若 ,说明装置不漏气。
③装置A中的试剂 ,装置C的作用 。
④以上实验装置存在明显缺陷,该缺陷导致测定结果偏高,该缺陷为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com