
题目列表(包括答案和解析)
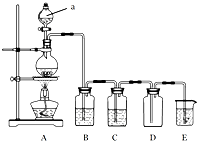 如图是实验室中制备气体或验证气体性质的装置图.
如图是实验室中制备气体或验证气体性质的装置图.
| ||
| ||
| ||
| ||
|
| 实验步骤 | 预期现象和结论 | |
| ① | 取少量上述漂白粉于试管中, 加入适量的1mol/L盐酸溶解后,将产生的气体通入足量的澄清石灰水中 加入适量的1mol/L盐酸溶解后,将产生的气体通入足量的澄清石灰水中 |
(1)若澄清石灰水未见浑浊,则假设1成立 (2)若澄清石灰水变浑浊,则假设2或3成立 (1)若澄清石灰水未见浑浊,则假设1成立 (2)若澄清石灰水变浑浊,则假设2或3成立 |
| ② | 向步骤①反应后的试管滴入1~2滴品红溶液,振荡 向步骤①反应后的试管滴入1~2滴品红溶液,振荡 |
(1)若品红褪色,固体中存在 Ca(ClO)2,假设3成立;(2)若品红不褪色,则固体中不存在 Ca(ClO)2,假设2成立; (1)若品红褪色,固体中存在 Ca(ClO)2,假设3成立;(2)若品红不褪色,则固体中不存在 Ca(ClO)2,假设2成立; |
| ③ | 此空不填写 此空不填写 |
此空不填写 此空不填写 |

| ||
| ||
某化学实验小组同学为了证明和比较SO2和氯水的漂白性,设计了如图所示的实验装置.
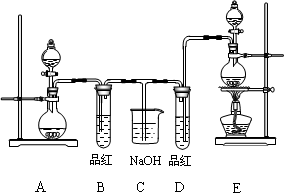
(1)实验室常用装置E制备Cl2,指出该反应中浓盐酸所表现出的性质:________.
(2)反应开始后,发现B、D两个试管中的品红溶液都褪去,停止通气后,给两个试管加热,两个试管中的现象分别为B:________,D:________.
(3)装置中C的作用是________.
(4)该实验小组的同学将SO2和Cl2先混合后通入品红溶液,通气一段时间后,品红溶液几乎不褪色,经测定品红溶液显强酸性.品红不褪色的原因:________(用化学方程式表示).
A.SO2和Cl2都能使品红溶液褪色
B.SO2能使品红溶液褪色,Cl2却不能
C.Cl2能使石蕊试液褪色,SO2却不能
D.SO2、Cl2都不能使石蕊试液褪色
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com