
题目列表(包括答案和解析)
下列离子方程式不正确的是
A.硫酸氢钠溶液中滴加Ba(OH)2溶液至呈中性
![]()
B.FeCl3溶液中加入足量的Na2S溶液: 2Fe3++3S2-==2FeS↓+S↓
C.0.05 mol/LCa(H2PO4)2溶液与0.15 mol/L NaOH以等体积混合:
![]() +9H2O
+9H2O
D.实验室用FeS与稀盐酸制取H2S气体:
S2-+2H+====H2S↑
![]() FeSO4+H2S↑
FeSO4+H2S↑
FeS为难溶于水的块状固体,H2S是微溶于水的气体,故可用启普发生器制取。为验证SO2既有还原性,又有氧化性,请用下图的仪器和试剂完成问题:
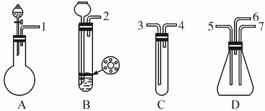
可选用的试剂:①盐酸 ②溴水 ③Na2SO3固体④FeS固体 ⑤品红试液 ⑥氢氧化钠溶液
(1)用乳胶管(图中未画出)连接上述仪器组合成一套实验装置,正确的连接顺序是(用导管口序号填空):______接______,______接______,______接______,______接尾气吸收装置。
(2)在装置A、B、C中应加入的试剂(用试剂序号填写)是: A______,B______,C______。
(3)表现SO2氧化性的实验是上述仪器中的______装置,实验中观察到的现象是______;表现SO2还原性的实验是上述仪器中的______装置,实验中观察到的现象是____________。
(4)整套装置最后的气体出口导管应连接_______,这样处理的理由是______________。

| 阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | -- | -- | -- |
| 沉淀完全时的pH | 3.7 | 11.1 | 8 | 9(>9溶解) |
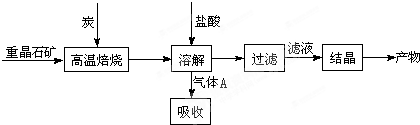
| 高温 |
| 高温 |
| c(Br-) |
| c(Cr-) |
| 高温 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com