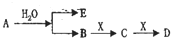(2013?保定一模)已知:A为淡黄色固体,E、X常温下为气体,A、B、C、D含有相同的 金属离子,其转化关系如图(部分产物已略去).
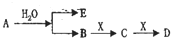
请回答下列问题:
(1)常温常压下,3.9gA与足量的氷充分反应放出热量akJ,写出该反应的热化学方程式
2Na2O2(s)+2H2O(l)=4NaOH+O2(g)△H=-4akJ/mol
2Na2O2(s)+2H2O(l)=4NaOH+O2(g)△H=-4akJ/mol
(2)向500mL0.3mol/L的B溶液中缓慢通入2.24L(标准状况下)的气体X,则 所得混合溶液中各离子浓度由大到小的顺序是
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
(3)已知20℃时的溶解度:“S(Na
2CO
3)=21.2g,S(NaHCO
3)=9.6g”.则20℃恒 温条件下向121.2g饱和碳酸钠溶液中通入足量的CO
2气体,理论上可以析出 NaHCO
324.3
24.3
g (小数点后保留1位).
(4)现有甲、乙两瓶无色溶液,已知它们可能是以下四种溶液:MgCl
2溶液、AlCl
3溶液、NaOH溶液、氨水中的两种,现做如下实验:
①取440mL甲与120mL乙反应,产生1.56g白色沉淀M
②取440mL乙与120mL甲反应,也产生1.56g白色沉淀M
③取120mL甲溶液与400mL乙溶液反应,则产生3.12g白色沉淀M;
通过必要的计算和推理判定:甲溶液为
AlCl3
AlCl3
溶液,乙溶液为
NaOH
NaOH
溶液.