
题目列表(包括答案和解析)
下图是A、B、C、D、E、F等几种常见有机物之间的转化关系图。其中A是面粉的主要成分;C和E反应能生成F,F具有香味。B与E的实验式相同
![]()
在有机物中,凡是具有-CHO结构的物质,具有如下性质:
(1)与新制的氢氧化铜悬浊液反应,产生砖红色的沉淀,
(2)在催化剂的作用下,-CHO被氧气氧化为-COOH,即:
2R-CHO+O2![]() 2R-COOH
2R-COOH
根据根据以上信息及各物质的转化关系完成下列各题:
(1) A的化学式为 ,B的结构简式为 。与B护卫同分异构体的一种物质的名称 。
(2) F在稀硫酸中发生水解反应的反应方程式
(3) E与氨水发生的离子方程式
E与小苏打溶液反应的化学方程式为
(4) 其中能与新制氢氧化铜悬浊液产生砖红色的沉淀的物质有 (填名称)。
(5) 写出钠与C的反应方程式
(6) 写出C→D的反应方程式
(7) C+E→F的反应方程式
 OH- + H+ 而碳化钙(CaC2)与水反应可以看作是一种复分解反应: CaC2 + 2H2O === Ca(OH)2 + C2H2↑
OH- + H+ 而碳化钙(CaC2)与水反应可以看作是一种复分解反应: CaC2 + 2H2O === Ca(OH)2 + C2H2↑ 
根据如图所示装置和下述操作方法,回答有关问题.
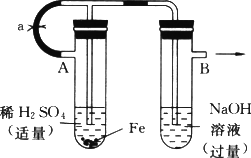
按如图所示装置,用两种不同的操作方法分别进行实验,观察B管中的现象.
(1)操作Ⅰ:先夹紧止水夹a,再使A管开始反应,实验中B管中观察到的现象是________,有关反应的离子方程式是________.
(2)操作Ⅱ:打开止水夹a,使A管反应一段时间后再夹紧止水夹a,实验中B管中观察到的现象是________,有关反应的离子方程式是________.
(3)请说明造成两种现象不同的原因(如两种现象相同,此小题不用回答)________.
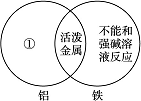
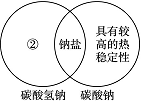
(1)下图是一种用于显示事物异同点的信息处理方法。例如A图中的两个圆分别代表铝和铁的有关信息,两圆重叠的区域表示铝和铁的共同点(相似点),重叠区域以外的部分表示它们独有的特征(不同点)。请你在下面横线上用化学方程式来表示与图中①②区域对应的化学性质上的不同之处(每处只要求写一个)。
 A
A
 B
B
①________________________________________________________________________;
②________________________________________________________________________;
(2)为了测定铁铝合金中金属的质量分数,某校研究性学习小组设计了如下实验操作过程:称取该合金1.0g,放入烧杯中加足量盐酸,盖上表面皿,使其充分反应;反应停止,经冷却向其中加入过量NaOH溶液,充分静置后过滤,对滤出的沉淀经洗涤在空气中加热灼烧至恒重,得到固体物质1.2g。下列有关叙述不正确的是________。
A.铁的质量为0.84g
B.Al的质量分数为16%
C.加入过量NaOH溶液的目的是为了Fe2+完全沉淀
D.加入NaOH溶液后充分静置是为了保证Fe(OH)2被空气中的氧气充分氧化为Fe(OH)3
(3)Al(OH)3和NaHCO3都是治疗胃酸过多的药物,用离子方程式表示其原理,________________,______________。根据上述反应,如果是胃酸过多且有胃溃疡的患者,应该选用上述哪一种药物治疗为好________,理由是________________________。

| 锥形瓶 | 胶头滴管 | 气球(A、B)的变化 | 有关反应的化学方程式 |
甲 | 二氧化硫 | 浓氢氧化钠溶液 |
|
|
乙 | 碳酸氢钠晶 | 体稀硫酸 |
|
|
(2)氯气是中学化学中常见的气体,可以用下图装置来制取。其中A装置可以加热,铁架台等其他仪器已略去。B中盛装的是饱和氯化钠溶液,D中盛装的是氢氧化钠溶液。?

①写出仪器名称:a ,b 。?
②写出实验室制取氯气的有关反应的化学方程式? ? 。?
③装置B的作用是 。?
装置D的作用是 。?
若装置C中盛装的溶液为FeCl2溶液,则通入氯气时发生反应的离子方程式为 。?
④利用该气体发生装置还可以制取其他气体,这些气体可以是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com