
题目列表(包括答案和解析)
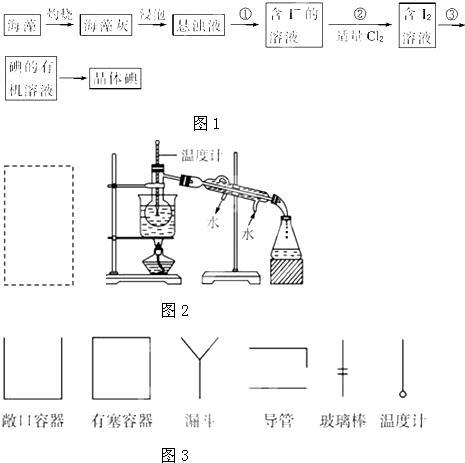
(4分)Ⅰ:一化学兴趣小组的同学通过如下实验提取海带中的碘:
①粉碎海带,加一定量的氢氧化钾溶液后高温灰化;②用水浸泡海带灰,过滤;③用盐酸酸化滤液,加入碘酸钾(KIO3)氧化溶液中的碘离子(I—),生成碘单质;④用四氯化碳溶液萃取水溶液中的碘。
请回答下列问题:
(1)实验步骤③中的离子反应方程式为
(2)实验步骤③中也可用H2O2代替KIO3,离子方程式为:
。
(3)检验用四氯化碳萃取碘后的水溶液是否还有碘单质的实验方法是 。
(共6分)II:从
| A.乙烯 | B.乙酸 | C.葡萄糖 | D.纤维素 E.油脂 |
(4分)Ⅰ:一化学兴趣小组的同学通过如下实验提取海带中的碘:
①粉碎海带,加一定量的氢氧化钾溶液后高温灰化;②用水浸泡海带灰,过滤;③用盐酸酸化滤液,加入碘酸钾(KIO3)氧化溶液中的碘离子(I—),生成碘单质;④用四氯化碳溶液萃取水溶液中的碘。
请回答下列问题:
(1)实验步骤③中的离子反应方程式为
(2)实验步骤③中也可用H2O2代替KIO3,离子方程式为:
。
(3)检验用四氯化碳萃取碘后的水溶液是否还有碘单质的实验方法是 。
(共6分)II:从A.乙烯 B.乙酸 C.葡萄糖 D.纤维素 E.油脂
F.蛋白质 六种有机物中选择合适的物质,将其字母序号填在空格内。
(1)属于烃类的是 。
(2)能与乙醇发生酯化反应的是 。
(3)植物通过光合作用直接生成的有机物是 。
(4)肉、蛋、奶等富含 。
(5)能作为制造肥皂的原料是 。
(6)棉花、甘蔗渣的主要成分是 。



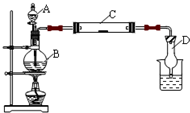 (2011?松江区模拟)为了制得氯气并探究氯气的一些化学性质,某学生用如图所示装置进行有关实验,打开A的玻璃塞,将A中浓盐酸溶液逐滴加入装有二氧化锰的B中.试回答:
(2011?松江区模拟)为了制得氯气并探究氯气的一些化学性质,某学生用如图所示装置进行有关实验,打开A的玻璃塞,将A中浓盐酸溶液逐滴加入装有二氧化锰的B中.试回答:
| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com