
题目列表(包括答案和解析)
A、某温度下
| ||
| B、常温下,pH=a的一元强酸溶液Va L与pH=b的二元强碱溶液Vb L混合,如果Vb:Va=10(14-a-b),则混合溶液一定呈中性 | ||
| C、某盐能够发生水解反应,将其加入水一定能促进水的电离 | ||
| D、将0.2 mol?L-1 HClO溶液和0.1 mol?L-1NaOH溶液等体积混合后,溶液显碱性,则此关系式:c(HClO)-c(ClO-)=2c(OH-)-2c(H+)一定正确 |
PCl3能与水发生如下发应:
PCl3+3H2O=H3PO3+3HCl,下列说法不正确的是
[ ]
A.该反应是氧化还原反应
B.该反应是复分解反应
C.PCl3是极性分子
D.PCl3与碱溶液反应生成多种盐
(1)下列说法不正确的是________(填字母序号)。
| A.60周年国庆阅兵车HQE顶级红旗采用全铝车身,铝的氧化物属于碱性氧化物 |
| B.用热的纯碱溶液洗涤沾有油污的器具时发生的主要是化学变化 |
| C.英国华裔科学家高锟因在“光在纤维中的传输应用于光学通信方面”做出了突破性成就,而获得了2009年诺贝尔物理学奖,光纤制品的基本原料为SiO2 |
| D.液氨、液氯、液态氯化氢都是非电解质 |
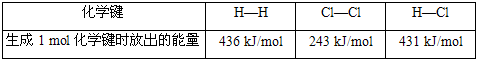
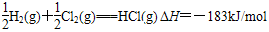
 CO2(g)+H2(g),在一定温度下,反应达到平衡后,得到0.6 mol二氧化碳,再加入2 mol水蒸气,在相同条件下达到新的平衡时二氧化碳的体积分数减小
CO2(g)+H2(g),在一定温度下,反应达到平衡后,得到0.6 mol二氧化碳,再加入2 mol水蒸气,在相同条件下达到新的平衡时二氧化碳的体积分数减小湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com