
题目列表(包括答案和解析)
下列说法正确的是
A.常温下,物质的量浓度均为0.1mol·L?1Na2CO3和NaHCO3的等体积混合溶液中:
2c(OH?)-2c(H+)=3c(H2CO3)+c(HCO3-)-c(CO32?)
B.ΔH<0,ΔS>0的反应都是自发反应,ΔH>0,ΔS>0的反应任何条件都是非自发反应;
C.已知:P4(g)+6Cl2(g)=4PCl3(g) ΔH=akJ·mol-1?
P4(g)+10Cl2(g)=4PCl5(g)ΔH= bkJ·mol-1
P4具有正四面体结构,PCl5中P-Cl键的键能为ckJ·mol-1,PCl3中P-Cl键的键能为1.2ckJ·mol-1,由此计算Cl-Cl键的键能

D.在一定温度下,固定体积为2L密闭容器中,发生反应:2SO2(g)+O2(g) 2SO3(g)
2SO3(g)
△H<0,当v(SO2)= v(SO3)时,说明该反应已达到平衡状态
| A.常温下,物质的量浓度均为0.1mol·L?1Na2CO3和NaHCO3的等体积混合溶液中: 2c(OH?)-2c(H+)=3c(H2CO3)+c(HCO3-)-c(CO32?) |
| B.ΔH<0,ΔS>0的反应都是自发反应,ΔH>0,ΔS>0的反应任何条件都是非自发反应; |
| C.已知:P4(g)+6Cl2(g)=4PCl3(g) ΔH=akJ·mol-1 P4(g)+10Cl2(g)=4PCl5(g)ΔH=bkJ·mol-1 P4具有正四面体结构,PCl5中P-Cl键的键能为ckJ·mol-1,PCl3中P-Cl键的键能为1.2ckJ·mol-1,由此计算Cl-Cl键的键能 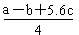 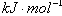 |
D.在一定温度下,固定体积为2L密闭容器中,发生反应:2SO2(g)+O2(g) 2SO3(g) 2SO3(g) |
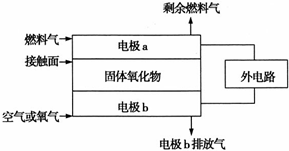 以氨作为燃料的固体氧化物(含有O2-)燃料电池,具有全固态结构、能量效率高的特点,其工作原理如图所示.下列说法正确的是( )
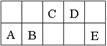
以氨作为燃料的固体氧化物(含有O2-)燃料电池,具有全固态结构、能量效率高的特点,其工作原理如图所示.下列说法正确的是( )下图是周期表中短周期的一部分。已知A、B两元素原子的最外层电子数之和等于E元素原子的最外层电子数。下列有关说法正确的是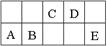
A.元素B和E、B和D形成的化合物在固态时都属于分子晶体
B.工业上可用A、D形成的化合物制取A的单质;B的单质在信息业有广泛用途
C.与E同族的元素中,若简单阴离子的还原性越强,则该元素的最高价氧化物对应水化物的酸性也越强
D.元素B的最简单氢化物分子的空间构型为正四面体,元素C的最简单氢化物的沸点比E的气态氢化物的沸点高
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com