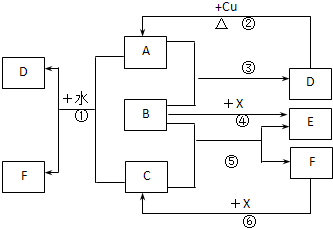
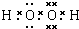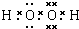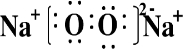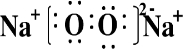(A)针对以下A~D四个涉及H
2O
2的反应(未配平),填写空白:
A.Na
2O
2+HCl→H
2O
2+NaCl
B.Ag
2O+H
2O
2→Ag+O
2+H
2O
C.H
2O
2→H
2O+O
2 D. H
2O
2+Cr
2(SO
4)
3+KOH→K
2CrO
4+K
2SO
4+H
2O
(1)H
2O
2仅体现氧化性的反应是(填代号)
D
D
,该反应配平的化学方程式为
3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O
3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O
.
(2)H
2O
2既体现氧化性又体现还原性的反应是(填代号)
C
C
.
(3)H
2O
2体现弱酸性的反应是(填代号)
A
A
,其理由为
这一反应可看作是强酸制取弱酸的反应
这一反应可看作是强酸制取弱酸的反应
.
(B)某学生利用以下装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置.

请回答下列问题:
(1)装置F中发生反应的离子方程式为
MnO
2+4H
++2Cl
-Mn
2++Cl
2↑+2H
2O
MnO
2+4H
++2Cl
-Mn
2++Cl
2↑+2H
2O
.
(2)装置A的烧瓶中可装试剂
生石灰或固体氢氧化钠
生石灰或固体氢氧化钠
.
(3)B装置的名称是
球形干燥管
球形干燥管
;E装置的作用
除去氯气中的HCl
除去氯气中的HCl
.
(4)通入C装置的两根导管左边较长、右边较短,目的是
使密度大的氯气与密度小的氨气较快地均匀混合
使密度大的氯气与密度小的氨气较快地均匀混合
.
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一.请写出反应的化学方程式:
3Cl2+8NH3═N2+6NH4Cl
3Cl2+8NH3═N2+6NH4Cl
.