
题目列表(包括答案和解析)
(13分)已知M是无色液体,C、H、D是有刺激性气味的气体,且D是单质,E为三原子非极性分子,②是工业上制取F的反应,J为漂白粉的有效成份。(部分反应条件未列出)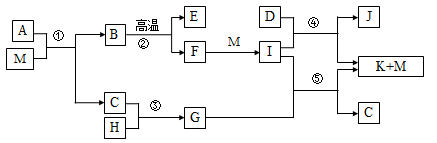
请回答下列问题:
(1)E、D、J的化学式分别是 、 、 ,G的电子式
(2)反应④的化学方程式
(3) 简述C的一种用途:
(4) A由三种元素组成,1 mol A与M反应可生成1 mol B和2 mol C,则A的化学式是
(5)漂白粉常用作消毒剂、杀菌剂、漂白剂等。漂白粉是一种混合物,漂白粉质量高低由"有效氯"(过量酸与漂白粉作用生成的氯气的质量与漂白粉的质量比)决定。漂白粉样品2.00克,加水研磨后,转入250毫升容量瓶内,用水稀释至刻度,摇匀后,取出25.0毫升,加入过量的KI溶液和过量的稀硫酸,静置。待漂白粉放出的氯气与KI完全反应后,用0.100摩/升的Na2S2O3标准溶液滴定反应中生成的碘。反应如下:2Na2S2O3+I2=Na2S4O6+2NaI滴定时用去Na2S2O3溶液20.0毫升。计算该漂白粉中有效氯的百分含量。
已知漂白粉与酸的反应为:Ca(ClO)2+CaCl2+2H2SO4=2CaSO4+2Cl2↑+2H2O
用实验证明![]() 、
、![]() 、
、![]() 氧化能力的顺序,简述操作过程,产生的现象和化学方程式(仪器可自行选用).实验药品可在下列药品中选用:锌片、铜片、ZnCl2溶液(0.1摩/升)、CuSO4溶液(0.1摩/升)、Hg(NO3)2溶液(0.1摩/升).
氧化能力的顺序,简述操作过程,产生的现象和化学方程式(仪器可自行选用).实验药品可在下列药品中选用:锌片、铜片、ZnCl2溶液(0.1摩/升)、CuSO4溶液(0.1摩/升)、Hg(NO3)2溶液(0.1摩/升).
(1)哪一支试管最先出现浑浊?哪一支试管最迟出现浑浊?为什么?
(2)另取三支试管A、B、C分别加入0.1摩/升Na2S2O3溶液5毫升,将A试管浸入冷水中,将B试管浸入热水中,而C试管置于室温条件下,然后再分别向这三支试管中加入0.1摩/升H2SO4溶液5毫升.问:哪一支试管最先出现浑浊?哪一支试管最迟出现浑浊?为什么?
氧化剂MO(OH)2+中的M元素的化合价+5,25毫升0.028摩/升的Na2SO3溶液恰好将含有2.8×10—4摩MO(OH)2+的溶液还原生成SO42-,则M元素的最终化合价为( )。
A. +2价 B. —2价 C. —1价 D. 0价
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com