
题目列表(包括答案和解析)
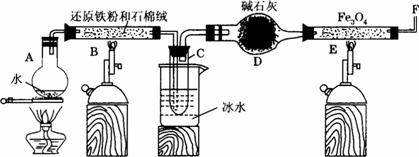
(1)为防止A中液体暴沸,可以采取的措施是___________;装置D能否改用盛有浓硫酸的洗气瓶___________。
(2)反应3Fe+4H2O(g)====Fe3O4+4H2↑在一定条件下实际为可逆反应,本实验中是如何实现Fe向Fe3O4的转变的?试用化学平衡移动原理加以解释__________________________________。
(3)停止反应,待B管冷却后,取其中固体加入过量稀盐酸,充分反应后过滤。简述证明滤液中含有Fe3+的实验操作及现象_____________________________________________________。
(4)若E管中反应按以下两步进行:Fe3O4+H2====3FeO+H2O,FeO+H2====Fe+H2O,假设实验开始时E管中的Fe3O4为23.
①Fe ②Fe租Fe3O4 ③FeO和Fe3O4 ④Fe和FeO ⑤Fe、FeO和Fe3O4
用此20 g固体与铝粉在一定条件下进行铝热反应,最多可消耗铝粉_________g(不考虑空气中的成分参与反应)。
| 1 | 2 |

某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用下图所示的装置先进行了有关实验:

⑴B是用来收集实验中产生气体的装置,但未将导管画全,请将装置图补充完整。
⑵实验中他们取6.4g铜片和12mL 18mol·L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①请写出铜与浓硫酸反应的化学方程式
②为什么有一定量的余酸但未能使铜片完全溶解?你认为原因是 。
③下列试剂中能够证明反应结束后的烧瓶中确有余酸的是 (填写字母编号)
A.铁粉 B.BaCl2溶液 C.银粉 D.Na2CO3溶液
(3)为了测定余酸的物质的量浓度,甲、乙两位同学进行了如下设计:
①甲同学设计方案是:先测定铜与浓硫酸反应产生的SO2的量,再计算余酸的物质的量浓度,他认为测定SO2的量的方法有很多种,请问下列实验方案中不可行的是 (填写字母编号)
A:将装置A产生的气体缓缓通过预先称量过的盛有碱石灰的干燥管,结束反应后再次称量
B:将装置A产生的气体缓缓通入足量用稀硫酸酸化的高锰酸钾溶液,再加入足量的氯化钡溶液,过滤、洗涤、干燥,称量沉淀
C:用排水法测定装置A产生气体的体积(已折算成标准状况)
D:将装置A产生的气体缓缓通入足量的氢氧化钡溶液(预先除去了溶解O2),反应完全后,过滤、洗涤、干燥,称量沉淀(隔绝空气条件下)
②乙同学设计的方案是:在反应后的溶液中加蒸馏水稀释至1000mL,取20mL于锥形瓶中,滴加2~3滴甲基橙指示剂,用标准氢氧化钠溶液进行滴定(已知:Cu(OH)2开始沉淀的pH约为5),通过测定出消耗NaOH溶液的体积来求余酸的物质的量浓度。假定反应前后烧瓶中溶液体积不变,你认为乙同学设计的实验方案能否求得余酸的物质的量浓度 ,(填能或否),其理由是 。
(4)请你再设计一个可行的实验方案来测定余酸的物质的量浓度。简要写出操作步骤及需要测定的数据,并写出相应的计算式。
(12分)气候变暖冰川融化将会对人类产生极大的灾害。如南极冰盖全部融化,南太平洋上的美丽岛国图瓦卢很可能成为首个“沉没”的国家,喜马拉雅山冰川融化尼泊尔会有“灭顶”之灾,近海城市遭受城市淹没、海啸等灾害。所以合理利用资源,加强环境保护。降低碳的排放,实施低碳经济是今后经济生活主流。
⑴下列措施对有效减少二氧化碳排放和降低大气中二氧化碳不适合的是 ▲
A.使用天然气等燃料
B.植树造林,保护森林,保护植被
C.大力发展风能、水力、潮汐能发电和核电,大力推行太阳能的综合开发
D.立即减少煤和石油化石燃料的使用
E.建筑物中尽量利用自然通风采光,推广使用节能灯和节能电器,使用空调时夏季温度不宜设置过低,冬天不宜过高
F.全民倡导出行时多步行和骑自行车;建设现代物流信息系统,减少运输工具空驶率
⑵目前用超临界CO2(其状态介于气态和液态之间)代替氟利昂作致冷剂已成为一种趋势,这一做法对环境的积极意义在于保护 ▲ 。
⑶科学家致力于二氧化碳的“组合转化”技术研究,把过多的二氧化碳转化为有益于人类的物质。如将CO2和H2以1∶4比例混合通入反应器,在适当条件下反应可获得一种重要能源。请完成以下化学方程式:CO2+4H2 = ▲ +2H2O
⑷收集提纯炼铁、炼钢等工厂所排放的气体,可得高纯度的CO,在适当的条件下,用CO和H2反应可获得人工合成汽油,也可减少碳的排放,节约能源。假设此人工合成汽油是碳原子数为5~8的烷烃,要达到合成汽油的要求,通入反应装置里的CO和H2的物质的量之比范围是 ▲ ≤n(CO)/n(H2) ≤ ▲ (保留最简分数比形式)
⑸探究CO2来生产燃料甲醇(CH3OH)的反应原理,现进行如下实验在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:
CO2(g)+3H2(g)CH3OH(g)+H2O(g)
测得CO2和CH3OH(g)的浓度随时间变化如下图所示。
从反应开始到平衡,氢气的平均反应速率v(H2)= ▲ 。
(12分)气候变暖冰川融化将会对人类产生极大的灾害。如南极冰盖全部融化,南太平洋上的美丽岛国图瓦卢很可能成为首个“沉没”的国家,喜马拉雅山冰川融化尼泊尔会有“灭顶”之灾,近海城市遭受城市淹没、海啸等灾害。所以合理利用资源,加强环境保护。降低碳的排放,实施低碳经济是今后经济生活主流。
⑴下列措施对有效减少二氧化碳排放和降低大气中二氧化碳不适合的是 ▲
| A.使用天然气等燃料 |
| B.植树造林,保护森林,保护植被 |
| C.大力发展风能、水力、潮汐能发电和核电,大力推行太阳能的综合开发 |
| D.立即减少煤和石油化石燃料的使用 |
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com