
题目列表(包括答案和解析)
根据反应(1)→(4),可以判断下列4个物质的氧化性由强到弱的正确顺序是:
⑴Cl2+2KI=2KCl+I2; ⑵2FeCl2+Cl2=2FeCl3;
⑶2FeCl3+2HI=2FeCl2+2HCl+I2,⑷H2S+I2=S+2HI;
A. S>I2>Fe3+>Cl2 B. Cl2>Fe3+>I2>S
C. Fe3+>Cl2>S>I2 D. Cl2>I2>Fe3+>S
 [化学-物质结构与性质]
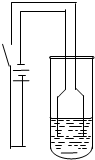
[化学-物质结构与性质] 某校化学研究性学习小组为探究铜及其化合物的性质,进行了如下科学探究:
某校化学研究性学习小组为探究铜及其化合物的性质,进行了如下科学探究:| 物质 | 性质 | 物质 | 性质 |
| 氯化铜 | 浓溶液呈绿色,稀溶液呈蓝色 | 氯化亚铜 | 白色 |
| 氧化亚铜 | 砖红色,在酸性条件下易反应: Cu2O+2H+=Cu+Cu2++H2O. Cu2O在空气中灼烧生成CuO | 氢氧化亚铜 | 橙黄色,不稳定 |
 (2010?祁阳县一模)某校化学研究性学习小组为探究铜及其化合物的性质,进行了如下科学探究:
(2010?祁阳县一模)某校化学研究性学习小组为探究铜及其化合物的性质,进行了如下科学探究:| 物质 | 性质 | 物质 | 性质 |
| 氯化铜 | 浓溶液呈绿色,稀溶液呈蓝色 | 氯化亚铜 | 白色 |
| 氧化亚铜 | 砖红色,在酸性条件下易反应: Cu2O+2H+=Cu+Cu2++H2O. Cu2O在空气中灼烧生成CuO |
氢氧化亚铜 | 橙黄色,不稳定 |
| ||
| ||
(13分)
第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物。
(1)①H、C、N、O四种元素的电负性由小到大的顺序为 。
②下列叙述不正确的是 。(填字母)
A.因为HCHO与水分子间能形成氢键,所以CH2O易溶于水
B.HCHO 和CO2分子中的中心原子均采用sp2杂化
C.C6H6分子中含有6个![]() 键和1个大
键和1个大![]() 键,C2H2是非极性分子
键,C2H2是非极性分子
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低
③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式 。
(2) Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是
②六氰合亚铁离子[Fe(CN)6]4-中不存在__________。
a、共价键 b、非极性键 c、配位键 d、σ键 e、π键
并写出一种与 CN_ 互为等电子体的单质分子式______________________。
③三氯化铁常温下为固体,熔点,沸点
,在
:以上升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁的晶体类型为___________。
(3)①Ti的在周期表中位置______________ 。
根据元素原子的外电子排布的特征,可将元素周期表分成五个区域,其中Ti属于 区。
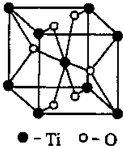
②Ti的一种氧化物X,其晶胞结构如上图所示,则X的化学式为 。工业上利用X和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐),制备M的化学反应方程式是________________________________________;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com