乙二胺四乙酸(EDTA)及其盐是常用于定量检测和分析金属离子的重要试剂.EDTA的阴离子可简写为Y
4-,它与一些金属离子反应生成稳定的金属有机化合物离子:M
2++Y
4-=(MY)
2-;M
3++Y
4-=(MY)
-.
试根据上述信息,回答下列问题.
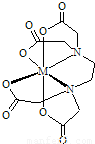
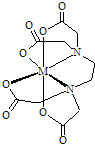
(1)(MY)
x- 的结构简式如图,该离子中与金属离子相连接的有6个共价键,则该离子结构中共含有
5
5
个五元环.
(2)现称取某铝盐试样0.2500g,将其溶于水后加入0.05000mol?L
-1 EDTA溶液25.00mL,在适当条件下充分反应后,调节溶液的pH为5~6,加入指示剂二甲酚橙,再用0.02000mol?L
-1的Zn(CH
3COO)
2溶液25.00mL 滴定至红色[Zn
2+遇二甲酚橙所显色,且Zn(CH
3COO)
2易电离],求该试样中铝元素的质量分数.
(3)按要求回答下列问题:①有一起始含0.01mol?L
-1的M
2+、0.5mol?L
-1 EDTA(Y
4-)和0.001mol?L
-1的S
2-的溶液,判断在该溶液中能否产生金属硫化物(MS)沉淀.
| M2+ |
K[(MY)2-] |
Ksp(MS) |
填“是”或“否” |
| Pb2+ |
2×1018 |
4×10-26 |
|
| Cd2+ |
2.6×1016 |
1×10-20 |
|
②以M
2+为Cd
2+为例,写出判断能否产生CdS沉淀的计算过程.
因为EDTA过量许多,若Cd
2+充分反应生成(MCd)
2-应为0.01mol?L
-1;假设(CdY)
2-的离解量为x,所以c[(CdY)
2-]=(0.01-x)mol?L
-1,c(Cd
2+)=xmol?L
-1,c(Y
4-)=(0.49+x)mol?L
-1;
因x<<0.01,所以K((CdY)
2-)=
| C((CdY) 2-) |
| c(Cd2+)×c(Y4-) |
=
≈
=2.6×10
16,
解得:x≈7.8×10
-18;
c(Cd
2+)?c(S
2-)=x?c(S
2-)=7.8×10
-18×0.001=7.8×10
-22<K
sp(CdS),所以不生成沉淀.
因为EDTA过量许多,若Cd
2+充分反应生成(MCd)
2-应为0.01mol?L
-1;假设(CdY)
2-的离解量为x,所以c[(CdY)
2-]=(0.01-x)mol?L
-1,c(Cd
2+)=xmol?L
-1,c(Y
4-)=(0.49+x)mol?L
-1;
因x<<0.01,所以K((CdY)
2-)=
| C((CdY) 2-) |
| c(Cd2+)×c(Y4-) |
=
≈
=2.6×10
16,
解得:x≈7.8×10
-18;
c(Cd
2+)?c(S
2-)=x?c(S
2-)=7.8×10
-18×0.001=7.8×10
-22<K
sp(CdS),所以不生成沉淀.
.

 乙二胺四乙酸(EDTA)及其盐是常用于定量检测和分析金属离子的重要试剂.EDTA的阴离子可简写为Y4-,它与一些金属离子反应生成稳定的金属有机化合物离子:M2++Y4-=(MY)2-;M3++Y4-=(MY)-.
乙二胺四乙酸(EDTA)及其盐是常用于定量检测和分析金属离子的重要试剂.EDTA的阴离子可简写为Y4-,它与一些金属离子反应生成稳定的金属有机化合物离子:M2++Y4-=(MY)2-;M3++Y4-=(MY)-.