
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
(3Зж)ДжбЮЬсДПЪЕбщжаЃЌГ§ШЅФрЩГЕФШ§ИіЛљБОВйзїЪЧЃК ЁЂ ЁЂ ЁЃ
ФГЦЗХЦЬЧвТЦЌВЙбЊМСЃЌГ§ШЅЬЧвТКѓЯдЕРЖТЬЩЋЃЌжївЊГЩЗжЪЧСђЫсбЧЬњЃЌВЛКЌЦфЫќЬњЕФЛЏКЯЮяЁЃФГбаОПадбЇЯАаЁзщЮЊВтЖЈИУВЙбЊМСжаСђЫсбЧЬњЕФКЌСПНјааСЫвдЯТЬНОПЃК
ЧыЛиД№ЯТСаЮЪЬтЃК
ЂёЃЎЃЈ1ЃЉЪЕбщЪБгУ18.4 molЁЄL-1ЕФХЈСђЫсЃЌХфжЦ100 mL 1 molЁЄL-1 H2SO4ШмвКЃЌЫљашХЈСђЫсЕФЬхЛ§ЮЊ ЁЃЃЈМЦЫуНсЙћОЋШЗЕНаЁЪ§ЕуКѓвЛЮЛЃЉ
ЃЈ2ЃЉЯТСаВйзїжаЃЌШнСПЦПЫљОпБИЕФЙІФмга (ЬюађКХ)ЁЃ
AЃЎХфжЦвЛЖЈЬхЛ§зМШЗХЈЖШЕФБъзМШмвК BЃЎГЄЦкжќДцШмвК
CЃЎгУРДШмНтЙЬЬхШмжЪ DЃЎГЃгУРДДњЬцСПЭВСПШЁвЛЖЈЬхЛ§ЕФвКЬх
ЃЈ3ЃЉдкЯТСаХфжЦЙ§ГЬЪОвтЭМжаЃЌгаДэЮѓЕФЪЧЃЈЬюаДађКХЃЉ ЁЃ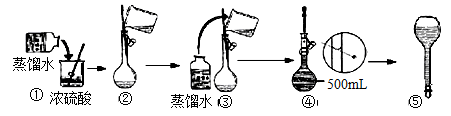
ЃЈ4ЃЉЯТСаЫЕЗЈе§ШЗЕФ
AЃЎЯДЕгЩеБ2~3ДЮЃЌВЂНЋЯДЕгвКвЦШыШнСПЦПвдМѕЩйЮѓВю
BЃЎФГЭЌбЇНЋХЈСђЫсЯЁЪЭКѓЮДРфШДжСЪвЮТБуНЋШмвКзЊвЦжСШнСПЦПЃЌЫљХфШмвКХЈЖШЛсЦЋЕЭ
CЃЎЖЈШнЪБбіЪгЙлВь,ЫљХфШмвКХЈЖШЛсЦЋЕЭ
DЃЎШнСПЦПЪЙгУЧАЯШвЊМьВщЪЧЗёТЉвКЃЌОпЬхВйзїЪЧЯђШнСПЦПжаМгеєСѓЫЎЃЌЕЙжУВЛТЉвКМДПЩ
ЂђЃЎЃЈ1ЃЉВНжшЂкМгШыЙ§СПH2O2ЕФФПЕФЃК ЁЃ
ЃЈ2ЃЉДгКьКжЩЋЕФаќзЧвКЕНзюКѓЕФГЦСПЃЌЦфЙ§ГЬжаЫљашЕФЛљБОВйзїЮЊЃК
a. ЃЌb. ЯДЕгЃЌc. зЦЩеЃЌd. РфШД
ЃЈ3ЃЉШєГЦЕУЙЬЬхЕФжЪСПЮЊagЃЌдђУПЦЌВЙбЊМСжаКЌСђЫсбЧЬњЕФжЪСПЮЊ ЁЃ
ЂѓЃЎвбжЊШЫЬхВЛФмКмКУЕиЮќЪеРћгУFe3+ЃЌПЦбЇбаОПБэУїЗўгУКЌСђЫсбЧЬњЕФВЙбЊМСЪБЃЌЭЌЪБЗўгУЮЌЩњЫиCЃЌвдРћгкЬњдЊЫиЕФЮќЪеЁЃЪдЗжЮіЮЌЩњЫиCдкетвЛЙ§ГЬжаЕФзїгУЪЧ ЁЃ
ФГЦЗХЦЬЧвТЦЌВЙбЊМСЃЌГ§ШЅЬЧвТКѓЯдЕРЖТЬЩЋЃЌжївЊГЩЗжЪЧСђЫсбЧЬњЃЌВЛКЌЦфЫќЬњЕФЛЏКЯЮяЁЃФГбаОПадбЇЯАаЁзщЮЊВтЖЈИУВЙбЊМСжаСђЫсбЧЬњЕФКЌСПНјааСЫвдЯТЬНОПЃК
ЧыЛиД№ЯТСаЮЪЬтЃК
ЂёЃЎЃЈ1ЃЉЪЕбщЪБгУ18.4 molЁЄL-1ЕФХЈСђЫсЃЌХфжЦ100 mL1 molЁЄL-1 H2SO4ШмвКЃЌЫљашХЈСђЫсЕФЬхЛ§ЮЊ ЁЃЃЈМЦЫуНсЙћОЋШЗЕНаЁЪ§ЕуКѓвЛЮЛЃЉ
ЃЈ2ЃЉЯТСаВйзїжаЃЌШнСПЦПЫљОпБИЕФЙІФмга (ЬюађКХ)ЁЃ
AЃЎХфжЦвЛЖЈЬхЛ§зМШЗХЈЖШЕФБъзМШмвК BЃЎГЄЦкжќДцШмвК
CЃЎгУРДШмНтЙЬЬхШмжЪ DЃЎГЃгУРДДњЬцСПЭВСПШЁвЛЖЈЬхЛ§ЕФвКЬх
ЃЈ3ЃЉдкЯТСаХфжЦЙ§ГЬЪОвтЭМжаЃЌгаДэЮѓЕФЪЧЃЈЬюаДађКХЃЉ ЁЃ
ЃЈ4ЃЉЯТСаЫЕЗЈе§ШЗЕФ
AЃЎЯДЕгЩеБ2~3ДЮЃЌВЂНЋЯДЕгвКвЦШыШнСПЦПвдМѕЩйЮѓВю
BЃЎФГЭЌбЇНЋХЈСђЫсЯЁЪЭКѓЮДРфШДжСЪвЮТБуНЋШмвКзЊвЦжСШнСПЦПЃЌЫљХфШмвКХЈЖШЛсЦЋЕЭ
CЃЎЖЈШнЪБбіЪгЙлВь, ЫљХфШмвКХЈЖШЛсЦЋЕЭ
DЃЎШнСПЦПЪЙгУЧАЯШвЊМьВщЪЧЗёТЉвКЃЌОпЬхВйзїЪЧЯђШнСПЦПжаМгеєСѓЫЎЃЌЕЙжУВЛТЉвКМДПЩ
ЂђЃЎЃЈ1ЃЉВНжшЂкМгШыЙ§СПH2O2ЕФФПЕФЃК ЁЃ
ЃЈ2ЃЉДгКьКжЩЋЕФаќзЧвКЕНзюКѓЕФГЦСПЃЌЦфЙ§ГЬжаЫљашЕФЛљБОВйзїЮЊЃК
a. ЃЌb. ЯДЕгЃЌc. зЦЩеЃЌd. РфШД
ЃЈ3ЃЉШєГЦЕУЙЬЬхЕФжЪСПЮЊagЃЌдђУПЦЌВЙбЊМСжаКЌСђЫсбЧЬњЕФжЪСПЮЊ ЁЃ
ЂѓЃЎвбжЊШЫЬхВЛФмКмКУЕиЮќЪеРћгУFe3+ЃЌПЦбЇбаОПБэУїЗўгУКЌСђЫсбЧЬњЕФВЙбЊМСЪБЃЌЭЌЪБЗўгУЮЌЩњЫиCЃЌвдРћгкЬњдЊЫиЕФЮќЪеЁЃЪдЗжЮіЮЌЩњЫиCдкетвЛЙ§ГЬжаЕФзїгУЪЧ ЁЃ
(3Зж)ДжбЮЬсДПЪЕбщжаЃЌГ§ШЅФрЩГЕФШ§ИіЛљБОВйзїЪЧЃК ЁЂ ЁЂ ЁЃ
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com