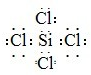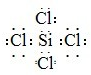(2012?东城区二模)四种短周期元素W、X、Y、Z,原子序数依次增大,请结合表中信息回答下列问题.
|
W |
X |
Y |
Z |
结构
或性质 |
最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物 |
焰色反应呈黄色 |
在同周期主族元素形成的简单离子中,离子半径最小 |
最高正价与最低负价之和为零 |
(1)Z在元素周期表中位于
IVA
IVA
族.
(2)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其它三种物质发生化学反应,该元素是
Na
Na
(填元素符号).
(3)①下列可作为比较X和Y金属性强弱的依据是
bc
bc
(填序号).
a.自然界中的含量 b.相应氯化物水溶液的pH
c.单质与水反应的难易程度 d.单质与酸反应时失去的电子数
②从原子结构的角度解释X的金属性强于Y的原因:
原子半径Na>Al,所以原子核对最外层电子的吸引力Na<Al,失电子能力Na>Al
原子半径Na>Al,所以原子核对最外层电子的吸引力Na<Al,失电子能力Na>Al
,原子半径X>Y,所以原子核对最外层电子的吸引力X<Y,失电子能力X>Y.
(4)W的一种氢化物HW
3可用于有机合成,其酸性与醋酸相似.体积和浓度均相等的HW
3与X的最高价氧化物对应的水化物混合,反应的化学方程式是
HN3+NaOH=NaN3+H2O
HN3+NaOH=NaN3+H2O
,混合后溶液中离子浓度由大到小的顺序是
c(Na+)>c(N3-)>c(OH-)>c(H+)
c(Na+)>c(N3-)>c(OH-)>c(H+)
.
(5)Y单质和Mg组成的混合物是一种焰火原料,某兴趣小组设计如下所示的实验方案,测定混合物中Y的质量分数.
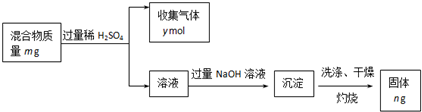
能确定混合物中Y的质量分数的数据有
abc
abc
(填序号).
a.m、n b.m、y c.n、y.

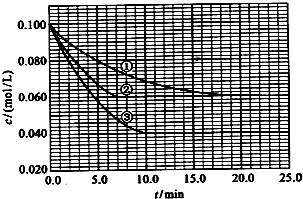 二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上可利用煤的气化产物(水煤气)合成二甲醚.
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上可利用煤的气化产物(水煤气)合成二甲醚.



 (2009?宿迁二模)聚合铁(简称PFS)化学式为:[Fe2(OH)n(SO4) 3-
(2009?宿迁二模)聚合铁(简称PFS)化学式为:[Fe2(OH)n(SO4) 3-