
题目列表(包括答案和解析)
某混合溶液由两种或三种物质溶于水制成,且在溶液中,c(K+)=c(C1-),c(Na+)=2c(SO![]() ),则溶质可能是………………………………………………………………( )
),则溶质可能是………………………………………………………………( )
A. KCl、Na2SO4 B. KCl、Na2SO4、NaCl
C. NaCl、Na2SO4、K2SO4 D. KCl、K2SO4、Na2SO4
A. KCl、Na2SO4 B. KCl、Na2SO4、NaCl
C. NaCl、Na2SO4、K2SO4 D. KCl、K2SO4、Na2SO4
| ||
| ||
(1)H
(2)若0.1 mol·L-1的NaHA溶液pH=3,则该溶液各离子浓度由大到小的顺序为________________;该溶液由水电离产生的c(H+)=_____________mol·L-1。
(3)往10 mL pH=3的 0.1 mol·L-1的NaHA溶液中加水至1 000 mL,溶液pH将___________。
A.等于5 B.大于
(4)在0.1 mol·L-1的NaHA溶液中离子浓度关系正确的是_____________。
A.c(HA-)+c(H
C.c(Na+)>c(HA-)>c(H+)>c(A2-) D.c(OH-) =c(H+)-c(A2-)
Ⅱ.在某压强恒定的密闭容器中加入2 mol N2和4 mol H2,发生如下反应:
N2(g)+3H2(g)![]() 2NH3(g);ΔH=-92.4 kJ·mol-1。达到平衡时,体积为反应前的三分之二。求:
2NH3(g);ΔH=-92.4 kJ·mol-1。达到平衡时,体积为反应前的三分之二。求:
(1)达到平衡时,N2的转化率为_____________。
(2)若向该容器中加入a mol N2、b mol H2、c mol NH3,且a、b、c均大于0,在相同条件下达到平衡时,混合物中各组分的物质的量与上述平衡相同,试比较反应放出的能量:
(1)_____________(2)(填“>”“<”或“=”)。
(3)若将2 mol N2和4 mol H2放入起始体积相同的恒容容器中(相同温度下),达到平衡。试比较平衡时NH3的浓度:(1)_____________(3)(填“>”“<”或“=”)。
(09盐城第三次调研)今有X、Y、Z三种有机物(其相对分子质量均小于100),它们含碳、氢、氧、氮4种元素中的三种或四种。有一合作学习小组的同学拟确定它们的组成或结构。
(1)测定有机物相对分子质量所用的方法通常是 (填序号,下同。①红外光谱,②质谱,③氢核磁共振谱,④
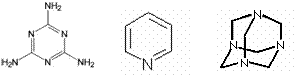
元素分析);下列物质的氢核磁共振谱只有一个吸收峰的是:
![]()
![]()
![]()
![]()
![]()
![]() (① 新戊烷, ② , ③ , ④ )
(① 新戊烷, ② , ③ , ④ )
![]()
![]() (2)X由C、H、O、N四种元素组成,ω(N)=18.67%,且X既能与盐酸反应又能与氢氧化钠溶液反应,则X可能的结构简式为: 。
(2)X由C、H、O、N四种元素组成,ω(N)=18.67%,且X既能与盐酸反应又能与氢氧化钠溶液反应,则X可能的结构简式为: 。
(3)Y和Z的相对分子质量相等,它们完全燃烧时,只能生成CO2、H2O、N2中的两种或三种。某同学取一定量的Y和Z的混合物,完全燃烧时在标准状况下的实验结果如下:
实验序号 | 混合物 质量 | 物质的量关系n(Y)/n(Z) | 产物的量 | ||
m(CO2)/g | m(H2O)/g | V(N2)/mL | |||
① | 3g | 2∶3 | 3.08 | 1.8 | 672 |
② | 3g | 3:2 | 3.52 | 1.8 | 448 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com