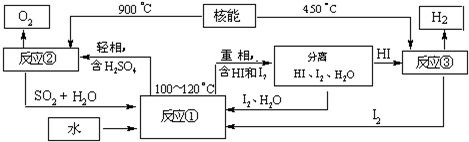
(2010?启东市模拟)某种芳香族化合物A,其蒸气密度是相同条件下H
2密度的82倍.A由碳、氢、氧三种元素组成,经测定碳、氢的质量分数分别为
73.2%和7.32%.
(1)A的分子式是
C10H12O2
C10H12O2
.
(2)已知:
ⅰ.

(R
1、R
2、R
3代表烃基)
ⅱ.

又知,A在一定条件下能发生如下转化,某些生成物(如H
2O等)已略去.

请回答:
①步骤Ⅰ的目的是
保护酚羟基
保护酚羟基
;
②若G为碳酸,则E的结构简式是
HCOOH
HCOOH
③F→H的反应类型是
缩聚反应
缩聚反应
;
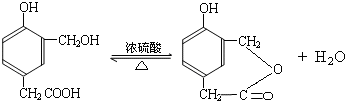
④F在一定条件下可发生酯化反应,生成M(M与FeCl
3反应,溶液呈紫色;且分子结构中含有苯环和一个七元环)请写出该反应的化学方程式
;
⑤A的结构简式是
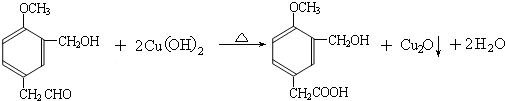
;上述转化中B→D的化学方程式是
.
(3)已知A的某种同分异构体N具有如下性质:
①N与FeCl
3反应,溶液呈紫色;
②N在一定条件下可发生银镜反应,N与H
2在苯环侧链上按照物质的量之比1:1作用后的生成物不能发生消去反应;
③在通常情况下,1mol N能与含1mol Br
2的浓溴水发生取代反应;
④N分子中苯环上的取代基上无支链.
请写出:N可能的结构简式
(写一种即可).
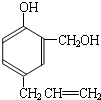
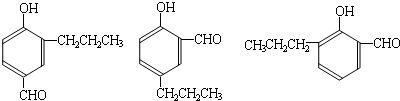
(4)请设计合理方案,完成从
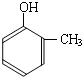
到的合成
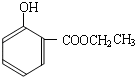
路线(用合成路线流程图表示,并注明反应条件).
提示:①;合成过程中无机试剂任选;②合成路线流程图示例如下:
CH
3CH
2OH
CH
2=CH
2

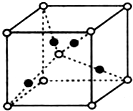 【化学一选修3物质结构与性质】
【化学一选修3物质结构与性质】 (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)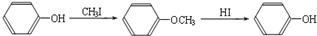









 (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)





 到的合成
到的合成 路线(用合成路线流程图表示,并注明反应条件).
路线(用合成路线流程图表示,并注明反应条件).