
题目列表(包括答案和解析)
X、Y、Z、是主族的三种非金属元素,它们在周期表中的位置如下图所示.试回答:

(1)X元素单质的化学式是______.
(2)Y元素的原子结构示意图是______,Y与Na所形成的化合物的化学式为______.
(3)Z元素的名称是______,从元素原子得失电子的角度看,Z元素具有______性;若从Z元素在周期表中所处位置看,它具有此性质的原因是______.
X、Y、Z、是主族的三种非金属元素,它们在周期表中的位置如下图所示.试回答:
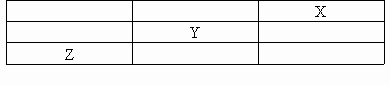
(1)X元素单质的化学式是______.
(2)Y元素的原子结构示意图是______,Y与Na所形成的化合物的化学式为______.
(3)Z元素的名称是______,从元素原子得失电子的角度看,Z元素具有______性;若从Z元素在周期表中所处位置看,它具有此性质的原因是______.




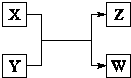 X、Y、Z、W四种物质有如右相互转化关系,X、W是同主族非金属元素组成的单质;W通常状况下是深红棕色液体;Y、Z是化合物的溶液;Y溶液呈淡绿色.
X、Y、Z、W四种物质有如右相互转化关系,X、W是同主族非金属元素组成的单质;W通常状况下是深红棕色液体;Y、Z是化合物的溶液;Y溶液呈淡绿色.
| ||
| ||
- 3 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com