
题目列表(包括答案和解析)
A.相同质量的O2、O3、O4含有相同的质子数
B.O4和O2、O3都属于同分异构体
C.合成O4的反应可看作核聚变反应,即不属于化学反应
D.O4分子内存在极性共价键
A.臭氧的同素异形体
B.氧元素的一种同位素
C.一种新的氧化物
D.可能是由极性键构成的分子
(6分)意大利科学家使用普通氧分子和带正电的氧离子作用,制出了新型的氧分子O4,它的结构很复杂,可能具有与S4相似的长方形结构,是一种高能量分子。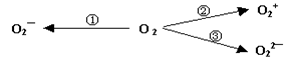
(1)下列有关O4的说法正确的是( )
| A.O4分子内存在极性共价键 |
| B.合成O4的反应不属于化学变化 |
| C.O4与O3、O2都是氧的同素异形体 |
| D.O4将来可用作更强有力的火箭推进的氧化剂 |
A.氧元素的一种同位素?
B.臭氧的同素异形体?
C.一种新的氧化物?
D.可能是由极性键构成的非极性分子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com