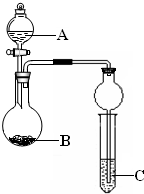
某同学设计了图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请回答:
(1)若A为浓氨水,B为烧碱,C为AlCl
3溶液,打开分液漏斗旋塞,烧瓶中即有氨气生成,
原因是
在氨水中有下列平衡:NH3+H2O?NH3?H2O?NH4++OH-,NaOH固体溶于水放热,使得氨气的溶解度减小,同时增大了溶液中的c(OH-),促使化学平衡逆向移动;
在氨水中有下列平衡:NH3+H2O?NH3?H2O?NH4++OH-,NaOH固体溶于水放热,使得氨气的溶解度减小,同时增大了溶液中的c(OH-),促使化学平衡逆向移动;
(结合离子方程式回答).一段时间后,观察到试管中的现象是
有白色沉淀产生
有白色沉淀产生
,
发生反应的离子方程是
Al3++3NH3?H2O=Al(OH)3↓+3NH4+
Al3++3NH3?H2O=Al(OH)3↓+3NH4+
.
(2)利用该装置设计实验证明醋酸、碳酸、苯酚的酸性强弱,若B为碳酸钠,A与B发生反应的离子方程式是
CO32-+2CH3COOH→2CH3COO-+H2O+CO2↑
CO32-+2CH3COOH→2CH3COO-+H2O+CO2↑
,能得到的相应结论是
醋酸酸性强于碳酸;
醋酸酸性强于碳酸;
;试管中出现浑浊,依据此现象能否得出相应的结论,请简述理由:
不能,因为醋酸具有挥发性,挥发出的醋酸也可以和苯酚钠溶液发生反应,生成苯酚
不能,因为醋酸具有挥发性,挥发出的醋酸也可以和苯酚钠溶液发生反应,生成苯酚
.


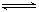 2CO2的平衡常数为K1;反应4Fe+3O2
2CO2的平衡常数为K1;反应4Fe+3O2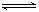 2Fe2O3的平衡常数K2,则反应3CO+Fe2O3
2Fe2O3的平衡常数K2,则反应3CO+Fe2O3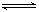 2Fe+3CO2的平衡常数K与K1、K2的关系式
2Fe+3CO2的平衡常数K与K1、K2的关系式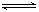 HSO3-+OH-
HSO3-+OH-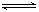 HSO3-+OH-
HSO3-+OH-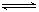 2AlCl3(g)+3CO(g)△H>0,欲提高金属铝的氯化效果,不可采取的措施是
2AlCl3(g)+3CO(g)△H>0,欲提高金属铝的氯化效果,不可采取的措施是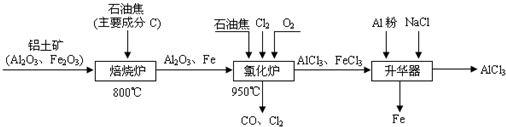
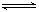
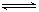
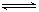
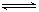











 中的-NH2可结合H2O电离出的H+,促进Al3++3H2O?Al(OH)3+3H+,向右移动,形成氢氧化铝沉淀
中的-NH2可结合H2O电离出的H+,促进Al3++3H2O?Al(OH)3+3H+,向右移动,形成氢氧化铝沉淀 中的-NH2可结合H2O电离出的H+,促进Al3++3H2O?Al(OH)3+3H+,向右移动,形成氢氧化铝沉淀
中的-NH2可结合H2O电离出的H+,促进Al3++3H2O?Al(OH)3+3H+,向右移动,形成氢氧化铝沉淀

 某同学设计了图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请回答:
某同学设计了图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请回答: