
题目列表(包括答案和解析)
在一个装有可移动活塞的容器中模拟传统工业合成氨的反应:N2(g)+3H2(g)![]() 2NH3(g),反应达到平衡后,测得NH3的物质的量为a mol
2NH3(g),反应达到平衡后,测得NH3的物质的量为a mol
(1)保持容器内的温度和压强不变,向平衡体系中又通入少量的H2,再次达到平衡后,测得NH3的物质的量为b mol,则a________b(填入“>”或“<”或“=”或“无法确定”,下同).若向平衡体系中通入的是少量N2,则a________b.
煤制油是一项
新兴的、科技含量较高的煤化工技术,发展煤制油对我国而言具有重大意义.下列是煤通过间接液化技术制汽油和丙烯的主要工艺流程图.
已知甲醇制烃的反应原理为:
(2)为了提高原料利用率,上述工艺中应控制合成气中V(CO)∶V(H2)=________.
(3)由二甲醚在催化剂作用下转化为丙烯的化学方程式为:________.
(4)每生产1 t甲醇约耗煤1.5 t,每生产1 t汽油约需耗2.4 t甲醇,2015年我国煤制油将达到1000万吨,则2015年当年需消耗原煤约________万吨.
(5)采用MTG法生产的汽油中,均四甲苯(1,2,4,5-四甲基苯)质量分数约占4%~7%,均四甲苯的结构简式为:________.
(6)采用DMTO技术,若获得乙烯和丙烯及丁烯3种烃,生成丁烯的选择性(转化丁烯的甲醇的物质的量与甲醇总物质的量之比)为20%,其余生成乙烯和丙烯,设丙烯的选择性为x,今有403.2 L(标准状况)合成气,且完全转化为甲醇,甲醇转化为烯烃的总转化率亦为100%,请作出丙烯的物质的量随x变化的曲线.
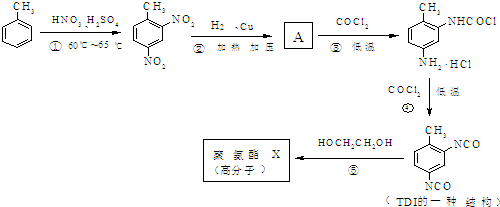
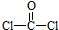
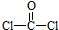
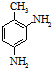

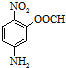

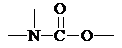 结构.第⑤步反应类型为
结构.第⑤步反应类型为








湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com