(2013?江西二模)以食盐为原料进行生产并综合利用的某些过程如图所示.
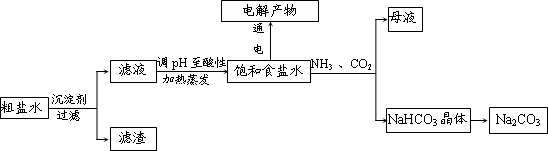
(1)除去粗盐中的Ca
2+、Mg
2+和SO
4-2离子,加入下列沉淀剂的顺序是(填序号)
cab或cba或bca
cab或cba或bca
.
a.Na
2CO
3 b.NaOH c.BaCl
2(2)将滤液的pH调至酸性除去的离子是
CO32-和OH-
CO32-和OH-
.
(3)电解氯化钠稀溶液可制备“84消毒液”,通电时氯气被溶液完全吸收,若所得消毒液仅含一种溶质,写出相应的化学方程式:
.
(4)若向分离出NaHCO
3晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的物质,其化学式是
NH3
NH3
.
(5)某探究活动小组将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如图所示(图中夹持、固定用的仪器未画出).
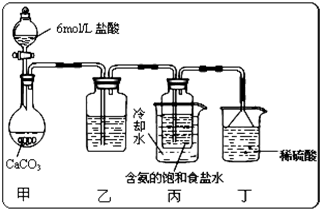
试回答下列有关问题:
①乙装置中的试剂是
饱和碳酸氢钠溶液
饱和碳酸氢钠溶液
;
②丁装置中稀硫酸的作用是
吸收未反应的氨气
吸收未反应的氨气
;
③实验结束后,分离出NaHCO
3 晶体的操作是
过滤
过滤
(填分离操作的名称).
(6)纯碱在生产生活中有广泛的应用.
①纯碱可用于除灶台油污.其原因是(结合离子方程式表述)
碳酸根离子水解显碱性,CO32-+H2O?HCO3-+OH-,油污在碱性条件下水解而被除去
碳酸根离子水解显碱性,CO32-+H2O?HCO3-+OH-,油污在碱性条件下水解而被除去
.
②工业上,可以用纯碱代替烧碱生产某些化工产品.如用饱和纯碱溶液与Cl
2反应制取有效成分为NaClO的消毒液,其反应的离子方程式是
2CO32-+Cl2+H2O=2HCO3-+Cl-+ClO-
2CO32-+Cl2+H2O=2HCO3-+Cl-+ClO-
.(已知碳酸的酸性强于次氯酸).




 HCO3-+OH-,与油污发生反应,达到去污目的
HCO3-+OH-,与油污发生反应,达到去污目的 HCO3-+OH-,与油污发生反应,达到去污目的
HCO3-+OH-,与油污发生反应,达到去污目的


