
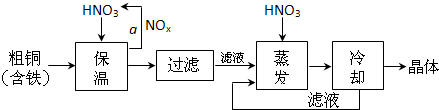
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
| ЗвСх»ҜОпҝӘКјіБөнКұөДpH | ЗвСх»ҜОпіБөнНкИ«КұөДpH | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
| H | + 4 |
| H | - 2 |
әПіЙ°ұИ»әуФЩЙъІъДтЛШКЗЧоЦШТӘөД»Ҝ№ӨЙъІъЎЈ
IЈ®ФЪ3ёц2 LөДГЬұХИЭЖчЦРЈ¬ФЪПаН¬өДОВ¶ИПВЎўК№УГПаН¬өДҙЯ»ҜјБ·ЦұрҪшРР·ҙУҰЈә
3H2(g) + N2(g) 2NH3(g)Ј¬°ҙІ»Н¬·ҪКҪН¶Ил·ҙУҰОпЈ¬ұЈіЦәгОВЎўәгИЭЈ¬ІвөГ·ҙУҰҙпөҪЖҪәвКұУР№ШКэҫЭИзПВЈә
2NH3(g)Ј¬°ҙІ»Н¬·ҪКҪН¶Ил·ҙУҰОпЈ¬ұЈіЦәгОВЎўәгИЭЈ¬ІвөГ·ҙУҰҙпөҪЖҪәвКұУР№ШКэҫЭИзПВЈә
|
|
јЧ |
ТТ |
ұы |
|
·ҙУҰОпН¶ИлБҝ |
3 mol H2Ўў2 mol N2 |
6 mol H2Ўў4mol N2 |
2 mol NH3 |
|
ҙпөҪЖҪәвөДКұјд/min |
|
5 |
8 |
|
ЖҪәвКұN2өДЕЁ¶И/molЎӨLЈӯ1 |
c1 |
1.5 |
|
|
NH3өДМе»э·ЦКэ |
ҰШ1 |
|
ҰШ3 |
|
»мәПЖшМеГЬ¶И/gЎӨLЈӯ1 |
ҰС1 |
ҰС2 |
|
ЈЁ1Ј©ИЭЖчТТЦР·ҙУҰҙУҝӘКјөҪҙпЖҪәвөД·ҙУҰЛЩВКОӘv(H2)=___________ЎЈ
ЈЁ2Ј©ФЪёГОВ¶ИПВјЧИЭЖчЦР·ҙУҰөДЖҪәвіЈКэK= (УГә¬c1өДҙъКэКҪұнКҫ)ЎЈ
ЈЁ3Ј©·ЦОцЙПұнКэҫЭЈ¬ПВБР№ШПөХэИ·өДКЗ________ЈЁМоРтәЕЈ©Јә
aЈ®2c1 > 1.5 bЈ®2ҰС1 = ҰС2 cЈ®ҰШ3 = ҰШ1
IIЈ®№ӨТөЙПУГ°ұЖшәПіЙДтЛШЈЁH2NCONH2Ј©өД·ҙУҰФЪҪшРРКұ·ЦОӘИзПВБҪІҪЈә
өЪТ»ІҪЈә2NH3(l)Ј«CO2(g) H2NCOONH4 (l) (°ұ»щјЧЛбп§)
ЎчH1
H2NCOONH4 (l) (°ұ»щјЧЛбп§)
ЎчH1
өЪ¶юІҪЈәH2NCOONH4(l) H2O(l)Ј«H2NCONH2(l)
ЎчH2
H2O(l)Ј«H2NCONH2(l)
ЎчH2
ЈЁ4Ј©ДіКөСйРЎЧйДЈДв№ӨТөЙПәПіЙДтЛШөДМхјюЈ¬ФЪТ»Ме»эОӘ0.5 LГЬұХИЭЖчЦРН¶Ил4 mol°ұәН1mol¶юСх»ҜМјЈ¬КөСйІвөГ·ҙУҰЦРёчЧй·ЦЛжКұјдөДұд»ҜИзЧуПВНјIЛщКҫЈә

ўЩТСЦӘЧЬ·ҙУҰөДҝмВэУЙВэөДТ»ІҪҫц¶ЁЈ¬ФтәПіЙДтЛШЧЬ·ҙУҰөДҝмВэУЙөЪ ІҪ·ҙУҰҫц¶ЁЎЈ
ўЪөЪ¶юІҪ·ҙУҰөДЖҪәвіЈКэKЛжОВ¶ИTөДұд»ҜИзУТЙПНјIIЛщКҫЈ¬ФтЎчH2 0Ј»ўЫИфөЪТ»ІҪ·ҙУҰЙэОВКұ°ұЖшЕЁ¶ИФцҙуЈ¬ЗлФЪНјIIЦР»ӯіцөЪТ»ІҪ·ҙУҰK1ЛжОВ¶ИTұд»ҜЗъПЯЈ¬ІўЧчіцұШТӘөДұкЧўЎЈ
ЈЁ5Ј©°ұәНДтЛШИЬТә¶јҝЙТФОьКХПх№ӨТөОІЖшЦРөДNOЎўNO2Ј¬Ҫ«ЖдЧӘ»ҜОӘN2ЎЈ
ўЩДтЛШУлNOЎўNO2ИэХЯөИОпЦКөДБҝ·ҙУҰОӘЈәCO(NH2)2+NO+NO2 =CO2+2N2+2H2O
ёГ·ҙУҰЦРөДСх»ҜјБОӘ ЈЁРҙ»ҜС§КҪЈ©ЎЈ
ўЪТСЦӘЈәN2(g)+O2(g)= 2NO(g) ЎчH =a kJЎӨmolЈӯ1
N2(g)+3H2(g)= 2NH3(g) ЎчH2=bkJЎӨ kJЎӨmolЈӯ1
2H2(g)+O2(g)= 2H2O(g) ЎчH = c kJЎӨmolЈӯ1
Фт4NH3(g) +4NO(g) +O2(g)= 4N2(g)+6H2O(g) ЎчH= ЎЈ
ўЫДтЛШИјБПөзіШҪб№№ИзПВНјЛщКҫЎЈЖд№ӨЧчКұёәј«өзј«·ҙУҰКҪҝЙұнКҫОӘ ЎЈ

Мјј°Жд»ҜәПОпУР№г·әөДУГНҫЎЈ
ЈЁ1Ј©Ҫ«Л®ХфЖшНЁ№эәмИИөДМјјҙҝЙІъЙъЛ®ГәЖшЎЈ·ҙУҰОӘЈә
C(s)Ј« H2O(g) 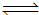 CO(g)
Ј«H2(g) ҰӨH=
+131.3 kJ•mol-1Ј¬ТФЙП·ҙУҰҙпөҪЖҪәвәуЈ¬ФЪМе»эІ»ұдөДМхјюПВЈ¬ТФПВҙлК©УРАыУЪМбёЯH2OөДЖҪәвЧӘ»ҜВКөДКЗ
ЎЈ(МоРтәЕ)
CO(g)
Ј«H2(g) ҰӨH=
+131.3 kJ•mol-1Ј¬ТФЙП·ҙУҰҙпөҪЖҪәвәуЈ¬ФЪМе»эІ»ұдөДМхјюПВЈ¬ТФПВҙлК©УРАыУЪМбёЯH2OөДЖҪәвЧӘ»ҜВКөДКЗ
ЎЈ(МоРтәЕ)
AЈ®ЙэёЯОВ¶ИЎЎ BЈ®ФцјУМјөДУГБҝ CЈ®јУИлҙЯ»ҜјБЎЎЎЎDЈ®УГCOОьКХјБіэИҘCO
ЈЁ2Ј©УЦЦӘЈ¬CЈЁsЈ©+ CO2ЈЁgЈ©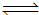 2COЈЁgЈ©
ЎчH=+172.5kJ•mol-1
2COЈЁgЈ©
ЎчH=+172.5kJ•mol-1
ФтCOЈЁgЈ©+H2OЈЁgЈ©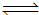 CO2ЈЁgЈ©+H2ЈЁgЈ©өДмКұдЎчH=
CO2ЈЁgЈ©+H2ЈЁgЈ©өДмКұдЎчH=
ЈЁ3Ј©COУлH2ФЪТ»¶ЁМхјюПВҝЙ·ҙУҰЙъіЙјЧҙјЈ¬COЈЁgЈ©+2H2ЈЁgЈ©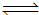 CH3OHЈЁgЈ©ЎЈјЧҙјКЗТ»ЦЦИјБПЈ¬ҝЙАыУГјЧҙјЙијЖТ»ёцИјБПөзіШЈ¬УГПЎБтЛбЧчөзҪвЦКИЬТәЈ¬¶аҝЧКҜД«Чцөзј«Ј¬ёГөзіШёәј«·ҙУҰКҪОӘЈә
ЎЈ
CH3OHЈЁgЈ©ЎЈјЧҙјКЗТ»ЦЦИјБПЈ¬ҝЙАыУГјЧҙјЙијЖТ»ёцИјБПөзіШЈ¬УГПЎБтЛбЧчөзҪвЦКИЬТәЈ¬¶аҝЧКҜД«Чцөзј«Ј¬ёГөзіШёәј«·ҙУҰКҪОӘЈә
ЎЈ
ИфУГёГөзіШМṩөДөзДЬөзҪв60mL NaClИЬТәЈ¬ЙиУР0.01molCH3OHНкИ«·ЕөзЈ¬NaClЧгБҝЈ¬ЗТөзҪвІъЙъөДCl2И«ІҝТзіцЈ¬өзҪвЗ°әуәцВФИЬТәМе»эөДұд»ҜЈ¬ФтөзҪвҪбКшәуЛщөГИЬТәөДpH=
ЈЁ4Ј©Ҫ«Т»¶ЁБҝөДCO(g)әНH2O(g)·ЦұрНЁИлөҪМе»эОӘ2.0LөДәгИЭГЬұХИЭЖчЦРЈ¬·ўЙъТФПВ·ҙУҰЈә
 CO(g)Ј«H2O(g)
CO2(g)Ј«H2(g)Ј¬өГөҪИзПВКэҫЭЈә
CO(g)Ј«H2O(g)
CO2(g)Ј«H2(g)Ј¬өГөҪИзПВКэҫЭЈә
|
ОВ¶И/Ўж |
ЖрКјБҝ/mol |
ЖҪәвБҝ/mol[С§ҝЖ |
ҙпөҪЖҪәвЛщxРиКұјд/min |
||
|
H2O |
CO |
H2 |
CO |
||
|
900 |
1.0 |
2.0 |
0.4 |
1.6 |
3.0 |
НЁ№эјЖЛгЗуіцёГ·ҙУҰөДЖҪәвіЈКэ(Ҫб№ыұЈБфБҪО»УРР§КэЧЦ) ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
ёДұд·ҙУҰөДДіТ»МхјюЈ¬·ҙУҰҪшРРөҪtminКұЈ¬ІвөГ»мәПЖшМеЦРCO2өДОпЦКөДБҝОӘ0.6 molЎЈИфУГ200 mL 5 mol/LөДNaOHИЬТәҪ«ЖдНкИ«ОьКХЈ¬·ҙУҰөДАлЧУ·ҪіМКҪОӘЈЁУГТ»ёцАлЧУ·ҪіМКҪұнКҫЈ©ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
ЈЁ5Ј©№ӨТөЙъІъКЗ°СЛ®ГәЖшЦРөД»мәПЖшМеҫӯ№эҙҰАнәу»сөГөДҪПҙҝH2УГУЪәПіЙ°ұЎЈәПіЙ°ұ·ҙУҰФӯАнОӘЈәN2(g)+3H2(g)
 2NH3(g)
ҰӨHЈҪ-92.4kJ•mol-1ЎЈКөСйКТДЈДв»Ҝ№ӨЙъІъЈ¬·ЦұрФЪІ»Н¬КөСйМхјюПВ·ҙУҰЈ¬N2ЕЁ¶ИЛжКұјдұд»ҜИзПВНјЎЈ
2NH3(g)
ҰӨHЈҪ-92.4kJ•mol-1ЎЈКөСйКТДЈДв»Ҝ№ӨЙъІъЈ¬·ЦұрФЪІ»Н¬КөСйМхјюПВ·ҙУҰЈ¬N2ЕЁ¶ИЛжКұјдұд»ҜИзПВНјЎЈ
І»Н¬КөСйМхјюПВ·ҙУҰЈ¬N2ЕЁ¶ИЛжКұјдұд»ҜИзПВНј1ЎЈ


Нј1 Нј2
Зл»ШҙрПВБРОКМвЈә
ўЩУлКөСйўсұИҪПЈ¬КөСйўтёДұдөДМхјюОӘ ЎЈ
ўЪКөСйўуұИКөСйўсөДОВ¶ИТӘёЯЈ¬ЖдЛьМхјюПаН¬Ј¬ЗлФЪЙПНј2ЦР»ӯіцКөСйўсәНКөСйўуЦРNH3ЕЁ¶ИЛжКұјдұд»ҜөДКҫТвНјЎЈ
ЈЁ10·ЦЈ©ОӘБЛәПАнАыУГ»ҜС§ДЬЈ¬И·ұЈ°ІИ«ЙъІъЈ¬»Ҝ№ӨЙијЖРиТӘід·ЦҝјВЗ»ҜС§·ҙУҰөД·ҙУҰИИЈ¬ІўІЙИЎПаУҰҙлК©ЎЈ»ҜС§·ҙУҰөД·ҙУҰИИНЁіЈУГКөСйҪшРРІв¶ЁЈ¬ТІҝЙҪшРРАнВЫНЖЛгЎЈ
ЈЁ1Ј©ҪсУРИзПВБҪёцИИ»ҜС§·ҪіМКҪЈә?Фтa bЈЁМо>,= , <Ј©
H2(g)+O2(g) ЈҪ H2O(g)ЎЎҰӨH1ЈҪa kJЎӨmol-1?
H2(g)+O2(g) ЈҪ H2O(l) ҰӨH2ЈҪb kJЎӨmol-1??
ЈЁ2Ј©УЙЖшМ¬»щМ¬ФӯЧУРОіЙ1mol»ҜС§јьКН·ЕөДЧоөНДЬБҝҪРјьДЬЎЈҙУ»ҜС§јьөДҪЗ¶И·ЦОцЈ¬»ҜС§·ҙУҰөД№эіМҫНКЗ·ҙУҰОпөД»ҜС§јьөДЖЖ»өәНЙъіЙОпөД»ҜС§јьөДРОіЙ№эіМЎЈФЪ»ҜС§·ҙУҰ№эіМЦРЈ¬ІрҝӘ»ҜС§јьРиТӘПыәДДЬБҝЈ¬РОіЙ»ҜС§јьУЦ»бКН·ЕДЬБҝЎЈ
| »ҜС§јь | HЈӯH | NЈӯH | NЎФN |
| јьДЬ/kJЎӨmolЈӯ1 | 436 | 391 | 945 |
ТСЦӘ·ҙУҰN2(g)Ј«3H2(g)2NH3(g) ЎчHЈҪa kJЎӨmolЈӯ1ЎЈКФёщҫЭұнЦРЛщБРјьДЬКэҫЭ№АЛгa өДЦөЈә_______________ЎЈ
ЈЁ3Ј©ТАҫЭёЗЛ№¶ЁВЙҝЙТФ¶ФДіР©ДСТФНЁ№эКөСйЦұҪУІв¶ЁөД»ҜС§·ҙУҰөД·ҙУҰИИҪшРРНЖЛгЎЈ
ТСЦӘЈәC(s)Ј«O2(g)ЈҪCO2(g) ЎчH1ЈҪЈӯ393.5kJЎӨmolЈӯ1
2H2(g)Ј«O2(g)ЈҪ2H2O(l) ЎчH2ЈҪЈӯ571.6kJЎӨmolЈӯ1
2C2H2(g)Ј«5O2(g)ЈҪ4CO2(g)Ј«2H2O(l) ЎчH3ЈҪЈӯ2599kJЎӨmolЈӯ1
ёщҫЭёЗЛ№¶ЁВЙЈ¬јЖЛг298KКұУЙC(s)әНH2(g)ЙъіЙ1molC2H2(g)·ҙУҰөД·ҙУҰИИ
ЎчH ЈҪ______________________ЎЈ
ПВБРИИ»ҜС§·ҪіМКҪЦРЈ¬ХэИ·өДКЗ
AЈ®јЧНйөДИјЙХИИОӘ890.3 kJЎӨmol-1Ј¬ФтјЧНйИјЙХөДИИ»ҜС§·ҪіМКҪҝЙұнКҫОӘЈә
CH4ЈЁgЈ©+2O2ЈЁgЈ©=CO2ЈЁgЈ©+2H2O(g) ЎчH=-890Ј®3 kJЎӨmol-1
BЈ®500ЎжЎў30MPaПВЈ¬Ҫ«0Ј®5mol N2ЈЁgЈ©әН1Ј®5molH2ЈЁgЈ©ЦГУЪГЬұХИЭЖчЦРід·Ц·ҙУҰЙъіЙNH3ЈЁgЈ©·ЕИИ19Ј®3 kJЈ¬ЖдИИ»ҜС§·ҪіМКҪОӘЈә
N2ЈЁgЈ©+3H2ЈЁgЈ© 2NH3ЈЁgЈ© ЎчH=-38Ј®6 kJЎӨmol-1
2NH3ЈЁgЈ© ЎчH=-38Ј®6 kJЎӨmol-1
CЈ®HClәНNaOH·ҙУҰөДЦРәНИИЎчH=-57.3 kJЎӨmol-1Ј¬ФтH2SO4әНCaЈЁOHЈ©2·ҙУҰөДЦРәНИИ
ЎчH=2ЎБЈЁ-57Ј®3Ј©kJЎӨmol-1
DЈ®ФЪ101 kPaКұЈ¬2gH2НкИ«ИјЙХЙъіЙТәМ¬Л®Ј¬·Еіц285Ј®8kJИИБҝЈ¬ЗвЖшИјЙХөДИИ»ҜС§·ҪіМКҪұнКҫОӘ2H2(g)+O2(g)=2H2O(1)ЎчH=-571Ј®6 kJЎӨmol-1
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com