
题目列表(包括答案和解析)
(12分)已知丙酮与柠檬醛在一定条件下反应可以合成假紫罗兰酮,再进一步可以合成有工业价值的紫罗兰酮,如: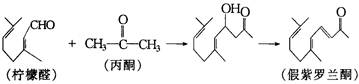
又知卤代烃可以发生水解
又知可发生下面反应: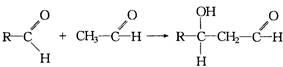 ,
,
下图是合成有机物A的路线图,反应条件和一些不必列出的产物等均已删去.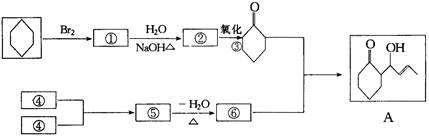
(1)写出结构简式
②________________⑤_________________⑥________________。
(2)写出化学方程式
①→②________________________ ④→⑤_________________________。
(12分)已知丙酮与柠檬醛在一定条件下反应可以合成假紫罗兰酮,再进一步可以合成有工业价值的紫罗兰酮,如:
又知卤代烃可以发生水解
又知可发生下面反应:,
下图是合成有机物A的路线图,反应条件和一些不必列出的产物等均已删去.
(1)写出结构简式
②________________⑤_________________⑥________________。
(2)写出化学方程式
①→②________________________ ④→⑤_________________________。
(12分)已知丙酮与柠檬醛在一定条件下反应可以合成假紫罗兰酮,再进一步可以合成有工业价值的紫罗兰酮,如:
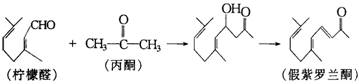
又知卤代烃可以发生水解
又知可发生下面反应: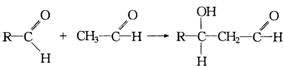 ,
,
下图是合成有机物A的路线图,反应条件和一些不必列出的产物等均已删去.
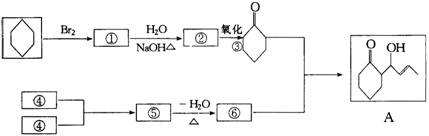
(1)写出结构简式
②________________⑤_________________⑥________________。
(2)写出化学方程式
①→②________________________ ④→⑤_________________________。
( 12分 ) 已知两个羧基之间在浓硫酸作用下脱去一分子水生成酸酐,如:

某酯类化合物A是广泛使用的塑料增塑剂。A在酸性条件下能够生成B、C、D。

( 1 ) CH3COOOH称为过氧乙酸,写出它的一种用途 _________ 。
( 2 ) 写出 B + E ![]() CH3COOOH + H2O 的化学方程式 ____________________ 。
CH3COOOH + H2O 的化学方程式 ____________________ 。
( 3 ) 写出F可能的结构简式 __________________ 。
( 4 ) 写出A的结构简式 ______________________ 。
( 5 ) 1 mol C分别和足量的金属Na、NaOH反应,消耗Na与NaOH物质的量之比是 _____ 。
( 6 ) 写出D跟氢溴酸 ( 用溴化钠和浓硫酸的混合物 ) 加热反应的化学方程式:
______________________________________________________ 。
(12分)已知2A2(g)+B2(g)
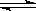 2C3(g);△H=-Q1 kJ/mol(Q1>0),在一个有催化剂的固定
2C3(g);△H=-Q1 kJ/mol(Q1>0),在一个有催化剂的固定
容积的容器中加入2 molA2和1 molB2,在500℃时充分反应,达平衡后C3的浓度为
w mol/L,放出热量Q2 kJ。
(1)若在原来的容器中,只加入2mol C3,500℃时充分反应达平衡后,吸收热量Q3 kJ,C3浓度 (填>、=、<)w mol/L,Q1、Q2、Q3 之间满足何种关系 (用代数式表示)。
(2)能说明该反应已经达到平衡状态的是 。
 a.v(C3)=2 v (B2); b.容器内压强保持不变
a.v(C3)=2 v (B2); b.容器内压强保持不变
c.v逆(A2)=2 v正(B2) d.容器内的密度保持不变
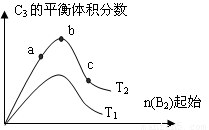
(3)改变某一条件,得到如图的变化规律(图中T表示温度,n表示物质的量),可得出的结论正确的是 ;
A.反应速率c>b>a
B.达到平衡时A2的转化率大小为:b>a>c
C.T2>T1
D.b点时,平衡体系中A、B原子数之比接近2∶1
(4)若将上述容器改为恒压容器(反应前体积相同),起始时加入2 molA2和l molB2,500℃时充分反应达平衡后,放出热量Q4 kJ,则Q2 Q4 ( 填 > 、 = 、 < ),理由是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com