
题目列表(包括答案和解析)
通常情况下空气中CO2的体积分数为0.030%,当空气中CO2的体积分数超过0.050%时,会引 起明显的温室效应。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
已知:CO2、碳酸盐、碳酸氢盐的部分性质如下:
CO2(过量)+OH一=HCO3- HCO3-+OH一=CO32一+H2O
CO32-+H+反应生成CO2分两步:
第一步:CO32-+H+= HCO3- 第二步:HCO3- +H+=CO2↑+ H2O
(1)目前,用超临界CO2( 其状态介于气态和液态之间)代替氟利昂作致冷剂已成为一种趋势,这一做法对保护环境的作用是 。
(2)最近有科学家提出“绿色自由’’构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,在一定条件下与H2反应,使之变为可再生燃料甲醇。其流程如下:
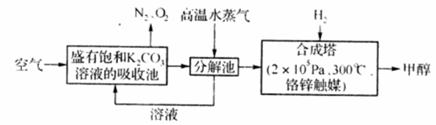
①写出CO2与H2反应制得甲醇的化学方程式: 。
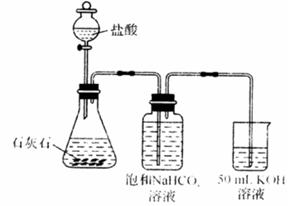
②某同学在实验室用下图所示的装置和药品制取K2 CO3溶液,他所制得的溶液中可能含有的杂质是
。
③某同学在数字化实验室中用传感器对碳酸钾和碳酸氢钾的混合物样品进行成分测定,他分别称取三份不同质量的混合物样品,配成溶液,然后逐滴加人相同浓度的稀硫酸,测得如下数据:

则该混合固体中K2CO3与KHCO3的物质的量之比是 ;所用硫酸的物质的量浓度为 。
通常情况下空气中CO2的体积分数为0.030%,当空气中CO2的体积分数超过0.050%时,会引起明显的温室效应。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
已知:CO2、碳酸盐、碳酸氢盐的部分性质如下:
CO2(过量)+OHˉ== HCO3 ˉ HCO3ˉ+OHˉ=CO32ˉ+H2O
CO32ˉ与H+反应生成CO2分两步:
CO32ˉ + H+ = HCO3 ˉ HCO3 ˉ+ H+ = CO2↑ + H2O
(1)目前,用超临界CO2(其状态介于气态和液态之间)代替氟利昂作致冷剂已成为一种趋势,这一做法对保护环境的作用是 。
(2)最近有科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,在一定条件下与H2反应,使之变为可再生燃料甲醇。其流程如下:
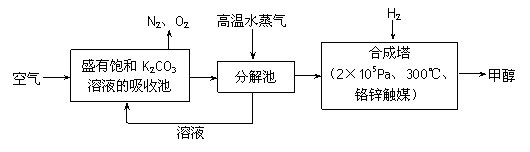

① 上述流程中碳酸钾溶液所起的作用是 。
②小李同学在实验室用右图所示的装置和药品制取
K2CO3溶液。他所制得的溶液中可能含有的杂质是
。
③小张同学在数字实验室中用传感器对碳酸钾和碳酸氢钾的混合物样品进行成分测定,他分别称取三份不同质量的混合物样品,配成溶液,然后用相同浓度的硫酸进行滴定, 测得如下数据:
| 实验编号 | 1 | 2 | 3 |
| 混合物的质量/g | 3.76 | 4.70 | 8.46 |
| 硫酸溶液的体积/mL | 50.00 | 50.00 | 50.00 |
| 生成二氧化碳的物质的量/mol | 0.03 | 0.0375 | 0.03 |
该混合固体中K2CO3与KHCO3的物质的量之比是 ;所用硫酸的物质的量浓度为: 。
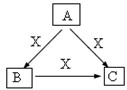 A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图.请针对以下三种不同情况回答:
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图.请针对以下三种不同情况回答:(15分) A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图。请针对以下三种不同情况回答:
(1)若A、B、C中均含同一种常见金属元素,该元素在 C中以阴离子形式存在,将A、C的水溶液混合可得B的白色胶状沉淀。
① A中含有的金属元素的原子结构示意图为 。
② 该金属元素的单质与某红色氧化物在高温下反应,可用于焊接铁轨及定向爆破,已知:1mol该单质完全反应,当温度恢复至298K时,共放热QkJ,请写出该反应的热化学反应方程式为 。
(2)若A为有机物,75%的A溶液可作为消毒剂,常温常压下B、C均为无色气体,C是一种常见的灭火剂。则A的结构简式为: ;利用原电池原理,将B、X分别通入由A制成的两多孔电极,以20%—30%的KOH溶液作为电解质溶液,可以组成化学电源,该电池放电时,负极电极反应式为 。
(3)若A、B、C的焰色反应均呈黄色,水溶液均为碱性。
①用化学方程式表明C溶液呈碱性的原因 。
②将4.48 L(标准状况下)X通入100 mL3 mol/L A的水溶液后,溶液中离子浓度由大到小的顺序为 。
③自然界中存在B、C和H2O按一定比例结晶而成的固体。取一定量该固体溶于水配成100 mL溶液,测得溶液中金属阳离子的浓度为0.5 mol/L。若取相同质量的固体加热至恒重,剩余固体的质量为___________________。
(15分) A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图。请针对以下三种不同情况回答:
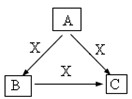
(1)若A、B、C中均含同一种常见金属元素,该元素在 C中以阴离子形式存在,将A、C的水溶液混合可得B的白色胶状沉淀。
① A中含有的金属元素的原子结构示意图为 。
② 该金属元素的单质与某红色氧化物在高温下反应,可用于焊接铁轨及定向爆破,已知:1mol该单质完全反应,当温度恢复至298K时,共放热QkJ,请写出该反应的热化学反应方程式为 。
(2)若A为有机物,75%的A溶液可作为消毒剂,常温常压下B、C均为无色气体,C是一种常见的灭火剂。则A的结构简式为: ;利用原电池原理,将B、X分别通入由A制成的两多孔电极,以20%—30%的KOH溶液作为电解质溶液,可以组成化学电源,该电池放电时,负极电极反应式为 。
(3)若A、B、C的焰色反应均呈黄色,水溶液均为碱性。
①用化学方程式表明C溶液呈碱性的原因 。
②将4.48 L(标准状况下)X通入100 mL3 mol/L A的水溶液后,溶液中离子浓度由大到小的顺序为 。
③自然界中存在B、C和H2O按一定比例结晶而成的固体。取一定量该固体溶于水配成100 mL溶液,测得溶液中金属阳离子的浓度为0.5 mol/L。若取相同质量的固体加热至恒重,剩余固体的质量为___________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com