
题目列表(包括答案和解析)

| 序号 | 气体 | 装置连接顺序(填字母) | 制备反应的化学方程式 | ||||||
| (1) | 乙烯 | B→D→E B→D→E |
CH3-CH2-OH
CH3-CH2-OH
| ||||||
| (2) | 乙炔 | A→C→E | CaC2+2H2O=Ca(OH)2+C2H2↑ CaC2+2H2O=Ca(OH)2+C2H2↑ |
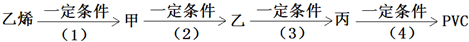
| 醇 |
| △ |
| 醇 |
| △ |
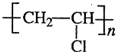
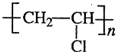
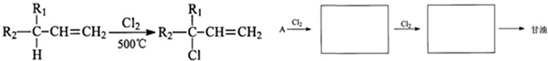
(14分)
I.在实验室利用下列装置,可制备某些气体并验证其化学性质。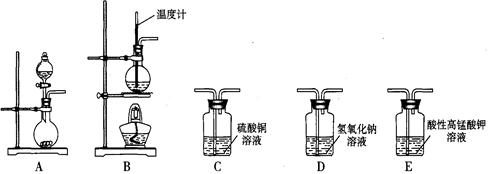
完成下列表格:
| 序号 | 气体 | 装置连接顺序(填字母) | 制备反应的化学方程式 |
| (1) | 乙烯 | __________________ | _________________________ |
| (2) | 乙炔 | A→C→E | _________________________ |
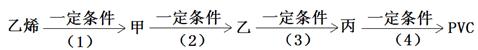
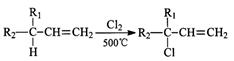
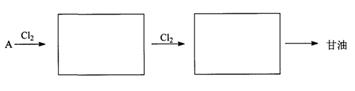
| 1 | 2 |


| 高温 |
| 高温 |
| 1 | 2 |

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com