
题目列表(包括答案和解析)
| I1 | I2 | I3 | I4 | … |
| 496 | 4562 | 6912 | 9540 | … |
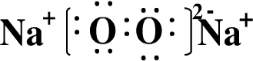
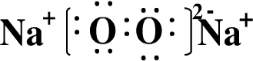
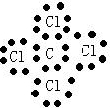

 X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y,X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物.
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y,X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物.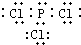
| 3 |
| 2 |
| 3 |
| 2 |

| 元素 | 相关信息 |
| X | 同素异形体之一自然界最硬 |
| Y | 与X同周期,且最高正价与最低负价代数和为2 |
| Z | 单质用于制黑火药,燃烧时有强烈的刺激性气味 |
| W | 基态原子只有一个未成对电子,单质及其合金 在潮湿的空气中容易出现绿色锈迹 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com