
题目列表(包括答案和解析)
 2H2O(g) △H=-483.6kj/mol
2H2O(g) △H=-483.6kj/mol  2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol  4NO(g)+6H2O(g) △H=-905kJ/mol
4NO(g)+6H2O(g) △H=-905kJ/mol  2N2(g)+6H2O(g)的△H=___________。如图是在一个密闭容器内,在催化剂作用下,一定量的氨气与氧气的混合气体在不同温度时的生成物及生成物含量与温度的关系图:温度较低时以反应_______(选填上述已知反应序号“①、②、③或④”)为主,当温度高于900℃时,NO产率下降的原因____。
2N2(g)+6H2O(g)的△H=___________。如图是在一个密闭容器内,在催化剂作用下,一定量的氨气与氧气的混合气体在不同温度时的生成物及生成物含量与温度的关系图:温度较低时以反应_______(选填上述已知反应序号“①、②、③或④”)为主,当温度高于900℃时,NO产率下降的原因____。 
 2NO2的化学平衡常数K=________。
2NO2的化学平衡常数K=________。 
 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,则平衡 移动(填“向左”“向右”或“不”);使用催化剂,上述反应的△H________(填“增大” “减小” 或“不改变”)。
2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,则平衡 移动(填“向左”“向右”或“不”);使用催化剂,上述反应的△H________(填“增大” “减小” 或“不改变”)。 式),生成该沉淀的离子方程式为____________。已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。
式),生成该沉淀的离子方程式为____________。已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。 中性,则Va︰Vb= 。
中性,则Va︰Vb= 。

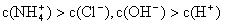

 NH3·H2O + H+,则该反应常温下的平衡常数K= (已知:常温下,NH3·H2O的电离平衡常数Kb=1.7×10—5 mol·L—1)
NH3·H2O + H+,则该反应常温下的平衡常数K= (已知:常温下,NH3·H2O的电离平衡常数Kb=1.7×10—5 mol·L—1)(16分)运用化学反应原理研究NH3的性质具有重要意义。请回答下列问题:
(1)已知:①4NH3(g)+3O2(g)===2N2(g)+6H2O(g) 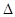 H=-1266.8kJ·mol-1
H=-1266.8kJ·mol-1
②N2(g)+O2(g)===2NO(g) 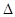 H=180.5kJ·mol-1
H=180.5kJ·mol-1
写出氨高温催化氧化的热化学方程式 。
(2)氨气、空气可以构成燃料电池,其电池反应原理为4NH3+3O2===2N2+6H2O。则原电解质溶液显 (填“酸性”、“中性”或“碱性”),负极的电极反应式为 。
(3)合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下: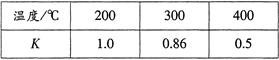
①由上表数据可知该反应为放热反应,理由是 ;
②理论上,为了增大平衡时H2的转化率,可采取的措施是 (填字母序号);
a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物中的NH3
③400oC时,测得某时刻氨气、氮气、氢气的物质的量浓度分别为3mol·L-1、2mol·L-1、1mol·L-1时,此时刻该反应的v正(N2) v逆(N2)(填“>”、“<”或“=”)。
(4)①25oC时,将amol·L-1的氨水与0.1mol·L-1的盐酸等体积混合。当溶液中c(NH4+)=c(Cl-)时,用含a的代数式表示NH3·H2O的电离常数Kb= ;
②向25mL0.10mol·L-1的盐酸中滴加氨水至过量,该过程中离子浓度大小关系一定不正确的是 (填字母序号)。
a.c(Cl-)>c(H+)>c(NH4+)>c(OH-) b.c(C1-)>c(NH4+)=c(H+)>c(OH-)
c.c(NH4+)>c(OH-)>c(Cl-)>c(H+) d.c(OH-)>c(NH4+)>c(H+)>c(Cl-)
 H=-1266.8kJ·mol-1
H=-1266.8kJ·mol-1 H=180.5kJ·mol-1
H=180.5kJ·mol-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com