
题目列表(包括答案和解析)
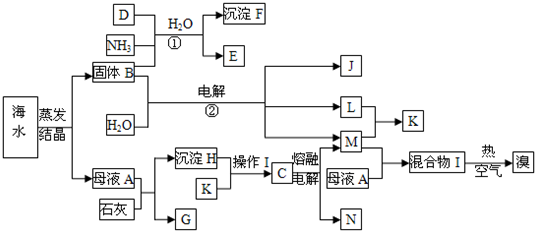
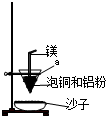 工业上冶炼冰铜(mCu2O?nFeS)可得到粗铜,再以粗铜为原料制备硫酸铜晶体.
工业上冶炼冰铜(mCu2O?nFeS)可得到粗铜,再以粗铜为原料制备硫酸铜晶体.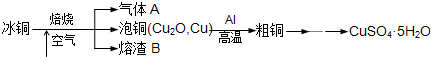
| ||
| ||
| 滴定剂 |
| 5bc |
| 4a |
| 5bc |
| 4a |
(20分)有一包从海水获得的粗盐,已经经过初步的提纯。课外活动小组对它的成分进行探究,并将粗盐进一步提纯。
探究一:这包粗盐中还有什么杂质?估计还含有氯化钙和氯化镁。
(1)现用实验验证推测:取样并溶解,加入几滴氢氧化钠溶液,目的是检验有没有___________________,接着再加数滴碳酸钠溶液,目的是检验有没有____________________。实验证明含有的杂质是氯化钙。
探究二:这包粗盐中氯化钠的质量分数是多少?接下面步骤继续实验:
①称取一定质量样品;
②将样品加水溶解;
③向粗盐溶液加入过量的某种试剂,过滤;
④沉淀洗涤后小心烘干,得到纯净固体A;
⑤滤液在进行某一操作后,移入蒸发皿蒸发,得到纯净固体B;
⑥称量实验中得到的某种固体。
(2)在②③⑤的步骤中,都使用到的同一仪器是____________,它在步骤②和⑤的操作方法相同,但目的不同,在步骤②的目的是_____________________,步骤⑤的目的是__________________________。(以上每空3分)
(3)在步骤③中加入的试剂是________________(2分)
(4)步骤⑥中,你认为需要称量的固体是A还是B____________,(1分)你不选择另一种的理由______________________。(2分)
(20分)有一包从海水获得的粗盐,已经经过初步的提纯。课外活动小组对它的成分进行探究,并将粗盐进一步提纯。
探究一:这包粗盐中还有什么杂质?估计还含有氯化钙和氯化镁。
(1)现用实验验证推测:取样并溶解,加入几滴氢氧化钠溶液,目的是检验有没有___________________,接着再加数滴碳酸钠溶液,目的是检验有没有____________________。实验证明含有的杂质是氯化钙。
探究二:这包粗盐中氯化钠的质量分数是多少?接下面步骤继续实验:
① 称取一定质量样品;
② 将样品加水溶解;
③ 向粗盐溶液加入过量的某种试剂,过滤;
④ 沉淀洗涤后小心烘干,得到纯净固体A;
⑤ 滤液在进行某一操作后,移入蒸发皿蒸发,得到纯净固体B;
⑥称量实验中得到的某种固体。
(2)在②③⑤的步骤中,都使用到的同一仪器是____________,它在步骤②和⑤的操作方法相同,但目的不同,在步骤②的目的是_____________________,步骤⑤的目的是__________________________。(以上每空3分)
(3)在步骤③中加入的试剂是________________(2分)
(4)步骤⑥中,你认为需要称量的固体是A还是B____________,(1分)你不选择另一种的理由______________________。(2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com